Перепрофилирование лекарств для лечения рака: комплексный обзор
Перепрофилирование лекарств для лечения рака: комплексный обзор
Рак входит в число основных причин глобальной смертности. В 2022 году число новых случаев рака в мире достигло около 20 миллионов, а число смертельных случаев, связанных с раком, достигло 9,7 миллиона. Перепрофилирование лекарств — это стратегия открытия лекарств, которая привлекла особое внимание и внедрение для улучшения процесса разработки лекарств из-за ее эффекта экономии времени и денег. Она включает в себя переориентацию существующих лекарств на новые клинические приложения. Лечение рака — это терапевтическая область, в которой повторное использование лекарств показало наиболее заметное влияние. В этом обзоре представлен сборник лекарств, которые были повторно использованы для лечения различных типов рака. В нем описаны начальные терапевтические и фармакологические классы повторно используемых лекарств, а также их новые применения и механизмы действия при лечении рака. В обзоре сообщается о препаратах из различных фармакологических классов, которые были успешно перепрофилированы для лечения рака, включая одобренные и находящиеся на стадии клинических испытаний и доклинической разработки. Он стратифицирует препараты на основе их перепрофилирования в противораковых целях как многотипные, типоспецифичные и направленные на механизм, а также в соответствии с их фармакологическими классами. В обзоре также рассматривается будущий потенциал перепрофилирования лекарств в клинической разработке новых методов лечения рака.
- ВВЕДЕНИЕ
Рак — это совокупность множества заболеваний, которые прогрессируют из-за неконтролируемой пролиферации клеток [1, 2]. Каждый тип имеет уникальные характеристики, но все они разделяют фундаментальные процессы, способствующие развитию заболевания [3, 4]. Раковые клетки могут быть злокачественными или нормальными, и они расширяются, когда им не поступают сигналы, игнорируя сигналы прекратить пролиферацию или подвергнуться апоптозу. Они направляют сосудистую пролиферацию в сторону злокачественных новообразований, обеспечивая кислородом и питанием, одновременно устраняя токсичные материалы. Они также избегают внимания иммунной системы, что облегчает их пролиферацию и выживание. Раковые клетки часто имеют разнообразный набор хромосомных модификаций, на которые они полагаются до такой степени, что не могут нормально функционировать [5].
Прогрессирование опухоли обычно иллюстрируется стадиями мутации и роста. Нормальная клетка трансформируется в злокачественную клетку с менее чем 10 мутациями [2, 6]. Стадии включают начальную мутацию, гиперплазию, дисплазию, рак in situ и инвазивные/злокачественные опухоли. Рак in situ характеризуется аномальным развитием и внешним видом клетки и ее потомства, в то время как инвазивные/злокачественные опухоли позволяют опухоли распространяться в другие ткани и выбрасывать клетки в лимфу или кровоток, потенциально порождая новые злокачественные опухоли.
Злокачественные опухоли могут распространяться по всему телу, вызывая резистентность к таргетной терапии [3]. Гены, критические для рака, делятся на две основные категории: протоонкогены и гены-супрессоры опухолей [ 7 ]. Протоонкогены способствуют пролиферации клеток, в то время как гены-супрессоры опухолей предотвращают ее. Мутации в этих генах могут приводить к повышенной активности белков, участвующих в путях стимуляции роста, заставляя клетки размножаться быстрее, чем без мутации [ 2 ].
Большинство злокачественных новообразований подразделяются на три основные категории: карциномы, саркомы и лейкемии или лимфомы. Карциномы составляют 90% случаев рака у человека, тогда как саркомы представляют собой солидные опухоли, поражающие соединительные ткани. Лимфомы и лейкемии вызываются иммунной системой и кроветворными клетками, составляя 8% всех злокачественных новообразований у человека. Опухоли далее классифицируются по типу клеток и тканевому происхождению [ 8 ].
Мутации и повреждения ДНК вызываются радиацией и химическими канцерогенами, которые считаются «стартовыми агентами», поскольку мутации в критических целевых генах являются самым ранним событием, ведущим к образованию рака (Рисунок 1). Канцерогенные химические вещества в табачном дыме, ультрафиолетовое излучение солнечного света и афлатоксин являются основными инициирующими агентами, способствующими возникновению рака у человека. Курение является причиной 80–90% злокачественных новообразований легких и связано с другими областями тела [ 9 ].
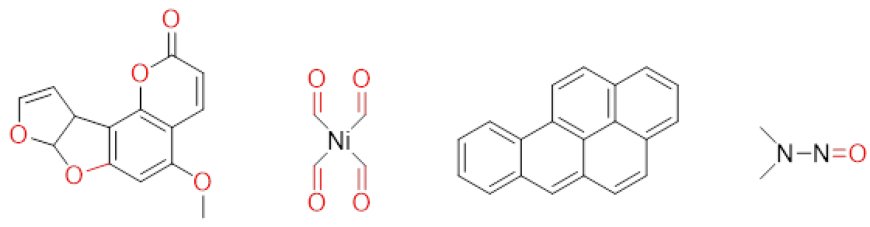
Рисунок 1. Иллюстрация химических канцерогенов,
вызывающих повреждение ДНК и мутации.
Гормоны, особенно эстрогены, могут способствовать возникновению некоторых злокачественных опухолей у человека, таких как рак эндометрия и рак молочной железы. Чрезмерное воздействие эстрогена увеличивает риск, в то время как терапия прогестероном может смягчить этот риск. Длительное использование комбинаций эстрогена и прогестерона также может увеличить риск рака молочной железы [ 10 ].
1.1 Проблемы, связанные с разработкой противораковых препаратов
Идеальный подход в фармакотерапии включает лекарства, которые точно нацелены и устраняют злокачественные клетки, сводя к минимуму побочные эффекты. Однако существенные различия между нормальными и раковыми клетками, такие как различия в активации сигнальных путей, чувствительность к гормонам или факторам роста и поведение роста, усложняют разработку эффективных методов лечения рака. Несмотря на эти проблемы, достижения в области эффективных лекарств, междисциплинарного и персонализированного лечения и улучшенных услуг паллиативной помощи, включая целевую терапию и мощные химиотерапевтические агенты, способствовали улучшению показателей выживаемости пациентов [ 16 ].
Несмотря на эти достижения, многочисленные неудачи в лечении сохраняются, в первую очередь из-за различных механизмов лекарственной устойчивости. Кроме того, стоимость новых методов лечения рака значительно возросла из-за обширных фармакологических исследований. Это финансовое бремя становится все более сложным для большинства систем здравоохранения, что требует инновационных подходов к перепрофилированию и улучшению существующих лекарств [ 16 ].
Стоимость лечения рака выросла примерно на 19%, 31% и 28% в 2020 году для начальной, текущей и конечной фаз терапии соответственно по сравнению с 2010 годом
[ 16 ]. Еще одной значительной проблемой в онкологических исследованиях является сложность рака, которая включает в себя многочисленные молекулярные модели с различной восприимчивостью и устойчивостью к различным методам лечения. Поэтому разработка более эффективных методов лечения рака имеет решающее значение [ 16 ].
1.2. Перепрофилирование лекарств
Повторное использование лекарств — одна из стратегий, которая находится в стадии обширных исследований и внедрения для решения этой проблемы [ 4 , 17 , 18 , 19 , 20 , 21 ]. Повторное использование лекарств — это использование уже одобренного лекарства для нового медицинского состояния или лечения, часто с использованием неожиданных побочных эффектов или неизвестных терапевтических эффектов [ 22 , 23 ]. Такой подход экономит время и деньги в фармацевтических исследованиях, обходя традиционный путь разработки лекарств и переходя к доклиническим и клиническим испытаниям [ 24 ]. Традиционная разработка лекарств известна своими длительными сроками и высокими затратами, часто требуя не менее 1 миллиарда долларов США и десяти лет, чтобы вывести новое лекарство на рынок [ 25 ]. Повторное использование лекарств фокусируется на быстром выявлении существующих лекарств, которые могут эффективно лечить состояния, выходящие за рамки их первоначального предполагаемого использования, особенно когда традиционная разработка лекарств de novo нецелесообразна или когда необходимы срочные терапевтические решения [ 26 ]. Существует несколько методов повторного использования лекарственных средств, включая разработку одобренных лекарственных средств для новых показаний, повторное использование одобренных и продаваемых молекул для использования не по назначению посредством клинических испытаний, а также спасение молекул, от которых отказались из-за таких проблем, как низкая эффективность или токсичность [ 27 ]. Регулирующие органы, такие как FDA, относят значительную часть вновь одобренных лекарств и биологических препаратов к перепрофилированию лекарств [ 28 ].
Применение повторного использования лекарств в терапии рака обеспечивает лучшие варианты смягчения для онкологических пациентов быстрее и с меньшими затратами за счет повторного использования неонкологических лекарств для борьбы с раковыми клетками. Различные методы были использованы для исследования потенциальных противораковых эффектов нераковых лекарств. Многочисленные исследования in vivo и in vitro с использованием линий раковых клеток и фармакологических моделей были проведены для изучения повторного использования неонкологических лекарств. Несколько всеобъемлющих электронных баз данных, включая Инициативу молекулярных библиотек и Национальные институты здравоохранения (NIH), были использованы для анализа химических соединений, биологических анализов и генетического значения активных химических соединений в контексте повторного использования лекарств.
Повторное использование неонкологических препаратов может происходить на любом уровне патофизиологических механизмов рака, включая индукцию апоптоза, ингибирование передачи сигналов и трансдукторов роста, ингибирование метаболизма раковых клеток, активацию противоопухолевого иммунитета, повторную активацию супрессоров роста, вмешательство в репликацию, снижение кровоснабжения опухоли и подавление инвазии и метастазирования [ 29, 30, 31, 32 ]. Однако повторное использование лекарств все еще имеет свои недостатки, включая барьеры интеллектуальной собственности, которые могут помешать дальнейшей разработке, и вероятность провала более высоких фаз клинических испытаний из-за более низкой эффективности по сравнению с текущей терапией или потенциальной токсичности для соответствующего дизайна клинического испытания.
- СЛУЧАИ ПЕРЕПРОФИЛИРОВАНИЯ ЛЕКАРСТВ ДЛЯ ЛЕЧЕНИЯ РАКА
В этом разделе будут описаны лекарства, которые были повторно использованы в лечении рака, насколько нам известно, и будет представлен отчет об их текущем статусе. Краткое изложение представлено в Таблице 1 , Таблице 2 и Таблице 3 .
2.1. Перепрофилирование с многотипной противораковой активностью
2.1.1. Перепрофилирование антитромбоцитарных препаратов для лечения рака
Аспирин, первоначально использовавшийся при сердечно-сосудистых заболеваниях, показал противоопухолевую активность и теперь перепрофилируется для лечения трижды негативного рака молочной железы. Исследования показали, что регулярное использование аспирина связано с более низким риском рака молочной железы. Было обнаружено, что аспирин подавляет рост клеток рака молочной железы с мутациями PIK3CA, активируя сигнальные пути, которые ингибируют mTORC1 и AMPK. Кроме того, вариации в SNP PIK3CA были связаны с различными результатами терапии аспирином у пациентов с раком молочной железы. В результате авторы [ 33 ] предположили, что сочетание ингибиторов PI3K с аспирином может быть эффективной стратегией лечения рака молочной железы, при условии, что пациенты стратифицированы на основе их генетического профиля относительно гена PI3K.
Аспирин ингибирует циклооксигеназы (ЦОГ), которые являются ферментами, участвующими в производстве простагландинов и тромбоксана, химических посредников, которые способствуют передаче болевых сигналов, свертыванию крови и воспалению. Уменьшая воспаление, аспирин может помочь предотвратить развитие и прогрессирование рака. Кроме того, аспирин может усилить противоопухолевую иммунную активность и поддержать другие противораковые иммунотерапии за счет снижения активности тромбоцитов. Исследования показали, что аспирин может ингибировать различные виды активности опухолевых клеток и нарушать микросреду опухоли, препятствуя росту и распространению раковых клеток [ 34 , 35 , 36 , 37 , 38 , 39 ].
Использование низких доз аспирина было связано со снижением риска различных видов рака, включая рак желудка, пищевода, колоректальный рак, рак поджелудочной железы, рак яичников, эндометрия, молочной железы и простаты. Однако метаанализ не обнаружил существенной разницы в заболеваемости раком или смертности между пользователями и не пользователями аспирина. Регулярное использование низких доз аспирина также было связано с улучшением показателей выживаемости, при этом исследования показали более низкий 10-летний риск рака и общую смертность по сравнению с не пользователями. После постановки диагноза рака использование низких доз аспирина было связано с более низкой смертностью у пациентов с раком пищеварительного тракта. Метаанализ восьми исследований обнаружил сильную корреляцию между использованием аспирина и снижением риска гепатоцеллюлярной карциномы, наиболее распространенного типа первичного рака печени. Использование низких доз аспирина также связано с 10% снижением риска развития рака яичников. Однако связь между использованием аспирина и выживаемостью у пациентов с раком яичников не была тщательно изучена [ 32 , 40 ].
2.1.2. Перепрофилирование противодиабетических препаратов для лечения рака
Несколько исследований задокументировали преимущества противодиабетических препаратов в лечении рака. Противодиабетические препараты из различных фармакологических классов и различных химических групп, включая классические группы, сульфонилмочевины, тиазолидиндионы, бигуаниды, а также недавние группы, ингибиторы натрий-глюкозного котранспортера-2 (SGLT2) и ингибиторы дипептидилпептидазы IV, эффективны при лечении некоторых видов рака. Считается, что метаболические связи между диабетом и раком, включая прямые эффекты, гипергликемию, гиперинсулинемию, и косвенные эффекты, воспаление, окислительный стресс и ожирение, способствуют противораковому действию этих препаратов.
Недавние исследования продемонстрировали, что противодиабетические препараты могут снижать возникновение рака, напрямую влияя на метаболизм раковых клеток и косвенно, изменяя маркеры, связанные с риском развития опухоли. Особое внимание было уделено сенсибилизаторам инсулина, включая метформин и группу тиазолидиндионов, из-за их впечатляющих результатов в клинических испытаниях. Метформин является основным средством лечения диабета 2 типа и широко признан как наиболее яркий пример. Многочисленные метаанализы исследований случай-контроль, когортных исследований, наблюдательных и клинических испытаний предоставили доказательства его эффективности в профилактике и лечении рака, независимо от того, используется ли он отдельно или в сочетании с другими лекарственными средствами. Метформин существенно снижает вероятность развития злокачественных новообразований толстой кишки, молочной железы, поджелудочной железы, предстательной железы, легких и шейки матки. Исследования показывают, что использование бигуанидов связано с 20–30%-ным снижением заболеваемости всеми видами рака и смертей, связанных с раком [ 41 , 42 ]. Тридцать семь клинических испытаний оценили метформин как самостоятельное лечение или в сочетании с традиционной терапией. Его эффективность против рака толстой кишки достигла фазы II и III клинических испытаний при использовании отдельно до и во время операции, а также в сочетании с традиционной терапией. Метформин вызывает остановку клеточного цикла в различных линиях клеток толстой кишки с помощью специфических механизмов [ 43, 44, 45, 46 ]. Метформин особенно эффективен в профилактике рака молочной железы, и в настоящее время более семи клинических испытаний оценивают его потенциал в качестве лечения рака молочной железы. Он достиг фазы III при использовании отдельно или в сочетании с аторвастатином и фазы II при сочетании с химиотерапевтическими препаратами, диетой или голоданием. Метформин подавляет раковые стволовые клетки (CSC) in vitro путем снижения регуляции генов, специфичных для CSC, и повторной экспрессии микроРНК. Он также снижает фосфорилирование pSTAT3, подавляет активность киназы S6 и mTOR, увеличивает AMPK и снижает трансляцию мРНК при раке молочной железы. Исследования показали, что метформин эффективно предотвращает рак кожи посредством нескольких механизмов. Например, метформин подавляет выработку TRB3 (tribbles pseudo kinase 3) in vivo, останавливая клетки меланомы в фазе G0/G1 и снижая рост и распространение меланомы. Кроме того, метформин активирует AMPK, влияя на микроокружение опухоли, а также на гибель и пролиферацию клеток меланомы. В различных линиях клеток меланомы метформин также снижает пролиферацию и инвазию клеток, модулируя ось miR-192-5p/EFEMP1 и miR-584 3p/SCAMP3 [ 47, 48, 49 ].
Как доклинические, так и клинические исследования продемонстрировали потенциал тиазолидиндионов (TZD) в лечении рака молочной железы и простаты. Основными компонентами этой категории являются троглитазон, розиглитазон и пиоглитазон. Эти соединения оказывают свое противораковое действие как через PPAR γ (рецептор, активируемый пролифератором пероксисом, гамма), так и через независимые пути. TZD стимулируют рецептор PPAR γ, который затем объединяется с ретиноидным X-рецептором, создавая гетеродимер. Это взаимодействие приводит к усилению апоптоза и дифференциации, а также к снижению деления популяции клеток. Таргетные цитотоксические препараты (TZD) зависят от экспрессии PTEN/AMPK, AKT/mTOR и распада циклинов D1 и D3, независимо от PPAR γ [ 50 , 51 ].
Хотя в настоящее время нет других антидиабетических методов лечения, проходящих исследования II фазы специально для рака толстой кишки, два фармакологических средства, десмопрессин и пиоглитазон, продемонстрировали эффективность против клеток рака толстой кишки различными методами. In vitro и in vivo десмопрессин, селективный агонист рецептора вазопрессина 2 (AVPR2), подавляет рост клеток рака толстой кишки. Снижая экспрессию COX-2 и циклина D1, пиоглитазон, синтетический лиганд PPAR, который повышает чувствительность к инсулину и гликемический контроль, подавляет метастазирование различных клеток рака толстой кишки [ 30, 52, 53, 54 ].
Механизм, посредством которого пиоглитазон вызывает остановку G0/G1 в клетках рака молочной железы MCF7, который частично зависит от PPAR и частично от MAPK, не был исследован в клинических испытаниях терапии рака молочной железы [ 55, 56, 57, 58 ].
Два противодиабетических препарата в настоящее время проходят клинические исследования для определения их эффективности в профилактике рака поджелудочной железы. Текущие испытания фазы II изучают использование пиоглитазона в сочетании с традиционными лекарствами, в то время как испытания фазы I изучают использование метформина в сочетании с дигоксином и симвастатином. Введение одного пиоглитазона усиливает выработку мРНК карциноэмбрионального антигена как в лабораторных условиях, так и в живых организмах. Кроме того, метформин сам по себе демонстрирует стимулирующее ингибирующее действие против нескольких клеток рака поджелудочной железы как в лабораторных условиях, так и в живых организмах [ 59, 60, 61 ].
2.1.3. Перепрофилирование противоглистных препаратов для лечения рака
Антипаразитарные препараты, такие как хлорохин и ивермектин, а также мебендазол, флубендазол и альбендазол, продемонстрировали потенциал в качестве противораковых средств. Эти препараты, изначально использовавшиеся для лечения кишечных паразитов, продемонстрировали противораковую активность, воздействуя на такие пути, как Wnt/β-катенин, NF-kB, сигнальные трансдукторы и активаторные транскрипционные белки [ 62, 63 ].
Флубендазол, известный бензимидазол, проявляет противоопухолевые свойства против различных видов рака, включая нейробластому, множественную миелому, лейкемию и рак молочной железы. Он вызывает апоптоз, генерацию активных форм кислорода и активацию каспазы 3 и 7. Флубендазол подавляет пролиферацию опухолей и образование новых кровеносных сосудов при раке легких, печени и молочной железы, избирательно атакуя раковые клетки, вызывая гибель клеток и усиливая экспрессию рецептора человеческого эпидермального фактора роста 2 (HER2) при раке молочной железы [ 64, 65, 66 ].
Ингибируя путь аутофагии, сигнальный преобразователь и транскрипционный белок 3, флубендазол оказывает летальное действие на колоректальный рак человека. Он также ингибирует пролиферацию клеток меланомы и метастазы, приводит к накоплению миелоидных супрессорных клеток и индуцирует запрограммированный белок смерти клеток-1 [ 67, 68 ].
Антигельминтики на основе бензимидазола также продемонстрировали противоопухолевые эффекты in vitro и in vivo в различных моделях рака, включая рак поджелудочной железы (РПЖ). Парбендазол, вводимый в терапевтических концентрациях в плазме, индуцирует апоптоз, нарушает клеточный цикл и запускает реакцию повреждения ДНК, ингибируя рост и клоногенность клеток РПЖ. Парбендазол значительно изменяет организацию микротрубочек в клетках РПЖ, что приводит к быстрому образованию полиплоидных клеток и аберрантным митотическим веретенам. Потенциал парбендазола дополнительно подчеркивается его синергетическим эффектом со стандартным химиотерапевтическим препаратом РПЖ гемцитабином. Биоинформационные инструменты выявили несколько неисследованных мишеней для бензимидазолов, связанных с раком, включая MAP-киназу p38 альфа, VEGFR2 и тирозин-протеинкиназу ABL, что указывает на необходимость дальнейших исследований in vitro и in vivo в РПЖ и других моделях опухолей для подтверждения этих результатов [ 52 ].
Мебендазол (MZ), обычно используемый для лечения кишечных паразитарных инфекций, ингибирует полимеризацию тубулина, что приводит к антипаразитарному эффекту. Как препарат для репозиционирования, мебендазол продемонстрировал синергические эффекты с темозоломидом при лечении злокачественных глиом, более эффективно подавляя рост опухоли, чем темозоломид в одиночку как в моделях ксенотрансплантата, так и в моделях сингенной глиомы. Мебендазол также демонстрирует синергические эффекты с доцетакселом в блокировании полимеризации тубулина, вызывая остановку митоза в фазе G2/M, увеличивая апоптоз и снижая пролиферацию клеток рака простаты и рост опухоли. Исследования in vivo и in vitro показывают, что мебендазол останавливает митотическую прогрессию в фазе G2/M, вызывает двухцепочечные разрывы и запускает апоптоз при раке молочной железы [ 69, 70 ].
Кроме того, мебендазол вызывает апоптоз, активируя путь каспазы-3, и предотвращает легочные метастазы при прогрессирующем раке щитовидной железы. Он также проявляет цитотоксичность при опухолях головного мозга и раке яичников, толстой кишки и эндокринной системы. Мебендазол вызывает апоптоз при холангиокарциноме, активируя каспазу 3, предотвращая деление клеток. Дополнительные исследования показывают, что мебендазол подавляет рост различных линий раковых клеток, включая глиобластому, медуллобластому, меланому, рак легких и колоректальный рак, как in vivo, так и ex vivo. Мебендазол вызывает апоптотическую гибель клеток при меланоме, активируя каспазы и проапоптотический Bcl-2, одновременно подавляя XIAP, регулятор апоптотического пути [ 71 ].
Более того, мебендазол проявляет высокое сродство к клеткам рака толстой кишки, что указывает на его потенциальную роль в качестве супрессора сигнализации Hedgehog в медуллобластоме и в качестве ингибитора киназ и онкогенов, таких как ABL и BRAF. У крыс, получавших мебендазол, наблюдается снижение роста опухоли и ангиогенеза, а также снижение частоты метастазов. Исследования случаев показывают, что терапевтическое введение мебендазола может иметь противораковые эффекты, причем одно раннее исследование показало замедление роста клеток рака легких без воздействия на фибробласты или нормальные эндотелиальные клетки. Пациенты с метастатическим колоректальным раком получали мебендазол после лечения первой и второй линии, испытывая минимальные побочные эффекты и значительное сокращение легочных и лимфатических метастазов, а также частичное восстановление печеночных метастазов. Пациенты с адренокортикальной карциномой, получавшие мебендазол после безуспешной химиотерапии, имели стабильное заболевание в течение примерно полутора лет, без побочных эффектов и с уменьшением размера метастазов [ 72 ].
Никлозамид, одобренный FDA противогельминтный препарат, как было показано, влияет на анаэробный метаболизм и абсорбцию глюкозы в клетках рака простаты, груди и яичников. Он также действует на увеличение трансдукции транскрипционных белков Wnt/β-катенина и NF-KB, влияя на различные сигнальные пути, включая метастазирование и активацию сигнала. Никлозамид значительно замедляет рост рака толстой кишки, печени и груди и предотвращает метастазирование клеток колоректального рака в печень и метастазов рака груди в легкие. Однако его клиническое развитие затруднено плохой растворимостью и более низкой биодоступностью, что может быть устранено путем внутривенного введения [ 73, 74 ].
Клиохинол, другой противопаразитарный препарат, продемонстрировал противораковые свойства, подавляя экспрессию HDAC в клетках лейкемии и злокачественной миеломы. Он вызывает апоптоз, подавляя HDAC и вызывая остановку митоза, что приводит к экспрессии p53 и p21 [ 75, 76 ].
2.1.4. Перепрофилирование противовирусных препаратов для лечения рака
Признанные своими противораковыми свойствами, антиретровирусные терапии (АРТ) могут вызывать отек клеток, апоптоз и изменение проницаемости мембран, что приводит к гибели клеток. АРТ запускают апоптоз, подавляют ангиогенез и повышают эффективность химиотерапии или облучения, производя токсичные свободные радикалы через реакцию, опосредованную двухвалентным железом. Активные формы кислорода (АФК), генерируемые АРТ, вызывают окислительное повреждение ДНК и апоптоз, делая раковые клетки более уязвимыми из-за отсутствия у них антиоксидантных ферментов. АРТ, в частности дигидроартемизинин, увеличивают АФК до возникновения цитотоксических эффектов, указывая на АФК как на основную причину повреждения клеток. АРТ нацелены на богатые железом раковые клетки, повышая их эффективность против опухолевых клеток с высокой экспрессией рецептора трансферрина (TfR). Исследования показывают, что АРТ в сочетании с аминоуксусным сульфатом железа повышает восприимчивость раковых клеток к АРТ, тогда как предварительная обработка дефероксамина мезилатом противодействует апоптозу, вызванному дигидроартемизинином, в лейкозных клетках [ 77 ].
Ингибиторы протеазы, используемые в антиретровирусной терапии, такие как ритонавир, нацелены на ВИЧ и показали противораковые эффекты при раке яичников, поджелудочной железы и молочной железы, вызывая апоптоз и подавляя рост раковых клеток. Ритонавир действует синергически с другими препаратами, включая темозоломид в клетках рака глиомы и бортезомиб в карциноме почки. Ритонавир продемонстрировал эффективность в лечении лимфоцитарного лейкоза и подавляет фосфорилирование Akt в клетках рака молочной железы [ 78, 79, 80 ].
Рибавирин — это противовирусный препарат на основе гуанозинового рибонуклеозида, который конкурирует с гуанилилтрансферазой и ингибирует 5′-мРНК, снижая уровень белка циклина D1 и ингибируя трансформацию онкогенов. Рибавирин также индуцирует трансляцию мРНК VEGF, подавляя прогрессирование человеческих лимфоцитов. Цидофовир, другой одобренный FDA противовирусный препарат, ингибирует вирусную ДНК-полимеразу и лечит различные вирусные инфекции, блокируя дифосфатные метаболиты. Он активирует каспазу и PARP в эпителиальных клетках, способствуя апоптозу и остановке митоза. Цидофовир ингибирует синтез ДНК и пролиферацию раковых клеток в клеточных линиях глиобластомы. Как in vitro, так и ксенотрансплантационные модели демонстрируют антипролиферативные свойства цидофовира, подавляя гены, связанные с апоптозом, в глиобластомах [ 81 ].
2.1.5. Перепрофилирование сердечно-сосудистых препаратов для лечения рака
Одобренные FDA сердечно-сосудистые препараты продемонстрировали потенциальные противораковые свойства в различных исследованиях.
- Лекарства от гипертонии
Лозартан, блокатор рецепторов ангиотензина (БРА), нормализует микросреду опухоли, истощая матрикс и снижая уровень коллагена I, подавляя рост опухоли и пролиферацию клеток. Лозартан показал многообещающие результаты в клинических испытаниях II фазы для лечения рака поджелудочной железы. Аналогичные механизмы используются другими БРА, такими как ирбесартан, валсартан, телмисартан и олмесартан. Каптоприл подавляет метастазы колоректального рака в печени, снижая жизнеспособность опухоли и препятствуя образованию метастазов. Было обнаружено, что карведилол подавляет инвазию и метастазирование клеток рака молочной железы, вмешиваясь в рецепторы факторов роста и функцию митохондрий [ 22, 82, 83 ].
Пропранолол, первый эффективный бета-блокатор, используется для лечения сердечных заболеваний, гипертонии и таких состояний, как инфантильные гемангиомы. Кумулятивные исследования показали, что бета-блокаторы, включая пропранолол, обладают антипролиферативными свойствами и могут подавлять распространение различных видов рака, таких как рак яичников, колоректальный рак, рак легких и рак простаты. Также наблюдались лучшие клинические результаты при множественной миеломе. Одна из гипотез заключается в том, что бета-блокаторы подавляют симпатическую нервную систему в нише костного мозга, тем самым улучшая клинические результаты для пациентов с множественной миеломой, особенно тех, кто переносит трансплантацию гемопоэтических стволовых клеток. Клинические испытания показывают, что пропранолол в сочетании с трансплантацией гемопоэтических стволовых клеток можно использовать для лечения множественной миеломы, несмотря на некоторые побочные эффекты, такие как головокружение, гипотония и гипокалиемия [ 84, 85 ].
Исследования показывают, что ингибиторы ЦОГ-2 и бета-блокаторы вместе могут замедлить прогрессирование заболевания при некоторых типах рака. Ингибиторы ЦОГ-2 оказывают антиангиогенное и апоптотическое действие, а некоторые виды рака, такие как почечно-клеточная карцинома, высвобождают простагландины, чтобы избежать эрадикации. Предоперационные бета-блокаторы в сочетании с ингибиторами ЦОГ-2 могут усилить иммунологический ответ и уменьшить метастазирование. У пациентов с первичным операбельным раком молочной железы, получавших пропранолол и этодолак, наблюдалось увеличение инфильтрирующих опухоль β-клеток, снижение инфильтрирующих опухоль моноцитов и снижение активности преметастатического/провоспалительного фактора транскрипции. Тошнота была наиболее частым нежелательным явлением, при этом не сообщалось об умеренных или тяжелых случаях [ 81, 86, 87 ].
Доклинические исследования показали, что некоторые антигипертензивные препараты повышают восприимчивость опухоли к химиотерапии, снижают пролиферацию клеток и действуют как коадъюванты против химиорезистентных клеточных линий при различных типах рака. Данные ретроспективного исследования показывают, что использование пропранолола в течение более 1000 дней снижает вероятность приобретения злокачественных новообразований в простате, толстой кишке, желудке и пищеводе. Дополнительные данные указывают на то, что статины, ингибиторы АПФ и БРА снижают вероятность рецидива рака молочной железы. Совместное применение сунитиниба с БРА и ингибиторами АПФ повышает общую выживаемость, частоту ответов и выживаемость без прогрессирования, а также снижает рецидив начального лечения у пациентов с почечно-клеточной карциномой [ 88, 89, 90 ].
Кандесартан и ирбесартан (БРА) являются ингибиторами ангиогенеза и васкуляризации опухоли в клеточных линиях рака толстой кишки. Кроме того, ирбесартан ингибирует связывание гена JUN и ДНК AP-1 у пациентов с метастатическим раком толстой кишки, что приводит к полному устранению при радиологическом тестировании. Эффективность ингибиторов АПФ, таких как каптоприл и эналаприл, в ингибировании превращения ангиотензина I в ангиотензин II была продемонстрирована против клеток рака толстой кишки как in vitro, так и in vivo. Эналаприл сам по себе снижает экспрессию IGF-IR 1 в сочетании с 5-фторурацилом и повышает радиочувствительность посредством активации пути NF-κB/STAT3. Хотя эналаприл в настоящее время не проходит клинических исследований, имеющиеся данные указывают на его перспективность в качестве модифицированной иммунотерапии рака. Блокатор кальциевых каналов нифедипин исключительно и избирательно подавляет экспрессию PDL-1 в клеточных линиях рака толстой кишки [ 83, 91, 92 ].
Восемнадцать клинических испытаний оценили пропранолол, неселективный бета-блокатор, отдельно или в сочетании с другими методами лечения различных видов рака, включая рак поджелудочной железы, нейробластому, ангиосаркому, рак молочной железы, рак легких, меланому и лейкемию. Пропранолол в сочетании с этодолаком в настоящее время проходит испытания II и III фазы для лечения колоректального рака. In vivo пропранолол снижает экспрессию p-AKT/p-ERK/p-MEK и стимулирует аутологичный CD8 + Т-клетки, тем самым подавляя колоректальный рак. В настоящее время проводятся два испытания фазы I для оценки воздействия пропранолола на рак яичников. Механизм его действия включает активацию защитной аутофагии и апоптоза через сигнальный путь JNK и ROS [ 93, 94 ].
Два антигипертензивных препарата находятся на стадии II испытаний при раке простаты: карведилол и пропранолол. Карведилол оценивается перед операцией, в то время как пропранолол исследуется до операции отдельно или с этодолаком. Ретроспективное исследование показывает, что долгосрочное использование атенолола значительно снижает риск рака простаты более чем на 50% [ 95, 96 ].
Исследования in vitro и in vivo показывают, что каптоприл и кандесартан подавляют клетки рака простаты, несмотря на то, что они не проходили клинических испытаний. Каптоприл увеличивает экспрессию p53, вызывая апоптоз в клетках рака простаты, в то время как кандесартан снижает рост опухоли и ангиогенез, ингибируя экспрессию VEGF. Гидралазин вызывает деметилирование в клетках рака простаты, повторно экспрессируя подавленные гены [ 97, 98 ].
В настоящее время проводится испытание фазы II для оценки миноксидила, прямого сосудорасширяющего антигипертензивного препарата, в качестве единственного лечения рака яичников. Активируя независимый от каспазы-3 путь клеточной смерти, он вызывает митохондриальные нарушения и существенное повреждение ДНК, тем самым изменяя метаболическое и окислительное состояние раковых клеток [ 99 , 100 ].
Активация миноксидилом пути гибели клеток, независимого от каспазы-3, приводит к нарушению работы митохондрий, существенному повреждению ДНК и изменениям в метаболическом и окислительном состоянии раковых клеток [ 101 ].
Хотя клинических испытаний, специально оценивающих их эффективность, не проводилось, четыре антигипертензивных препарата, включая каптоприл, телмисартан, ирбесартан и кандесартан, продемонстрировали многообещающие результаты в борьбе с раком печени и почек как в исследованиях in vitro, так и in vivo. Телмисартан и ирбесартан подавляют пролиферацию клеток рака печени, подавляя экспрессию pErbB3 и фосфорилируя p38/MAPK, тем самым снижая экспрессию VCAM-1 ниже по течению [ 102 ].
Телмисартан запускает апоптоз в почках или клеточных линиях рака почек, увеличивая экспрессию каспазы-3 и Bax, одновременно снижая экспрессию Bcl-2 (путь PI3/AKT). Кроме того, каптоприл подавляет пролиферацию клеток рака почек SN12K-1 в лабораторных и животных моделях [ 103 ].
Было показано, что тезосентан обладает потенциалом служить новым противораковым средством, ингибируя рецепторы эндотелина, которые сверхэкспрессируются в различных раковых клетках.
Кроме того, тезосентан продемонстрировал многообещающие доклинические результаты в ингибировании пролиферации раковых клеток и индукции апоптоза, особенно в злокачественных новообразованиях с самой высокой экспрессией рецептора эндотелина типа А [ 104 , 105 ].
- Перепрофилирование антигиперлипидемических препаратов
Фенофибрат, изначально разработанный для лечения гиперлипидемии, продемонстрировал противораковые свойства при различных типах рака у человека. Фенофибрат активирует AMPK, снижает уровень АТФ и увеличивает накопление ROS, что приводит к апоптозу и ингибированию метастазирования в раковых клетках. Фенофибрат также способствует апоптозу и остановке клеточного цикла, модулируя рецепторы факторов роста и активность NF-κB при раке груди, а также ингибируя сигнализацию ERK при раке легких. Противораковые эффекты фенофибрата не зависят от PPARα, что делает его потенциальным кандидатом для повторного использования в лечении рака [ 106 , 107 ].
- Перепрофилирование модуляторов ионных каналов для лечения рака
Ионные каналы играют важную роль в специфических возбудимых клетках, таких как сердечные миоциты и нейроны. Изучение роли ионных каналов в патофизиологии различных заболеваний привело к разработке лекарств, воздействующих на эти каналы. Прорывное исследование, подчеркивающее роль K + Каналы в митогенезе и онкогенезе вызвали интерес к их потенциалу в качестве мишеней для лечения рака. Следовательно, ионные каналы теперь считаются потенциальными терапевтическими мишенями, поскольку они влияют на рост раковых клеток посредством различных механизмов, включая регулирование мембранного потенциала и критические сигнальные пути выживания, такие как Ca 2+ и На + /К + [ 108 , 109 , 110 ].
На разных стадиях клеточного цикла раковые клетки испытывают изменения объема, контролируемые в первую очередь ионами, такими как калий, кальций, натрий и хлорид. Раковые клетки используют поток воды в ограниченных областях для продвижения себя во время миграции, а каналы аквапоринов облегчают прохождение воды между клетками. Согласно «модели осмотического двигателя», AQP5 (аквапорин 5) и NHE-1 (Na + /ЧАС + обменник-1) поляризуются на переднем крае клетки во время миграции, позволяя воде входить спереди и выходить сзади, что приводит к смещению клетки [ 111 , 112 ].
С 77 генами, кодирующими К + каналы, они очень разнообразны, и любой член этого большого семейства может быть дисрегулирован при определенном типе рака. Среди них каналы Kv10.1 (EAG1) были тщательно изучены и часто активируются в раковых клетках. Поэтому специфические блокаторы для этих различных K + Каналы необходимы для оптимального функционирования, что открывает возможность индивидуального лечения. Выявление нерегулируемых K + канал у пациента позволяет проводить лечение с помощью специфического ингибитора этого К + Член семейства каналов. Например, Kv10.1 экспрессируется примерно в 70% случаев рака, но практически отсутствует в органах, не относящихся к ЦНС, что делает менее опасным воздействие на эти каналы в опухолях, чем в нормальных тканях [ 113 , 114 ].
Хотя Kv10.1 практически отсутствует в здоровых тканях, отличных от ЦНС, он значительно повышен в нескольких линиях раковых клеток, таких как нейробластома, карцинома шейки матки, меланома и рак молочной железы. Повышенная экспрессия Kv11.1 (hERG) наблюдается в линиях клеток лейкемии человека. Каналы Kv10.1 заметно повышены в опухолевых тканях пациентов, таких как саркома мягких тканей (70%), рак шейки матки (100%), глиомы (Kv10.1 и Kv11.1), рак эндометрия (Kv11.1) и хронический лимфоцитарный лейкоз (Kv11.1), по сравнению с нераковыми клетками. После проведения обширного анализа более 470 клинических образцов опухолей было установлено, что Kv10.1 был повышен в 15 из 17 различных типов карциномы [ 115 , 116 ].
Доклинические исследования противораковых эффектов ингибирования калиевых каналов в первую очередь фокусируются на каналах Kv10.1, Kv10.2 (EAG2) и Kv11.1. Существующие препараты, такие как антиаритмический верапамил, противоэпилептический ретигабин и антидиабетические сульфонилмочевины, известны своим ингибирующим действием на калиевые каналы, такие как KATP, Kv11.1 и KCNQ соответственно.
Препараты сульфонилмочевины, такие как глипаламид, показали эффективность против меланомы, рака легких, желудка и молочной железы. Верапамил, антиаритмический препарат, эффективен против нейробластомы и рака простаты. Его сочетание ингибирующего действия на калиевые и кальциевые каналы способствует его противораковому эффекту. Астемизол, первоначально разработанный как антагонист H1, теперь демонстрирует потенциал в качестве противоракового препарата из-за его способности ингибировать Kv10.1. Текущие исследования показывают, что блокаторы калиевых каналов могут быть повторно использованы в качестве противораковых препаратов [ 117 , 118 ].
Блокаторы кальциевых каналов (БКК) Т-типа могут останавливать клеточный цикл в фазах G1 или S и повышать его восприимчивость к химиотерапии. Сочетание БКК с существующими препаратами повышает их эффективность. Кроме того, БКК блокируют p-гликопротеины, которые способствуют множественной лекарственной устойчивости раковых клеток [ 102 , 119 , 120 ].
Мибефрадил, кальциевый ингибитор T- и L-типа 2+ блокатор каналов, изначально продавался как антигипертензивное средство, но был отозван из-за взаимодействия с другими препаратами. Модификации мибефрадила могут создать более селективный Т-тип Ca 2+ блокаторы каналов с меньшим ингибированием CYP450 3A4, что потенциально улучшает их использование в терапии рака. TAU Therapeutics LLC перепозиционировала мибефрадил для лечения опухолей глиомы высокой степени злокачественности с помощью Interlaced Therapy TM, объединив его с темозоломидом для повышения эффективности химиотерапевтического препарата в активных клетках S-фазы. Этот подход в настоящее время проходит клинические испытания фазы 1b для подтверждения его эффективности [ 4 , 121 ].
2.1.6. Перепрофилирование антибиотиков для лечения рака
Антибиотики исследуются на предмет их потенциала воздействия на раковые клетки в дополнение к лечению бактериальных инфекций. Некоторые антибиотики, включая противотуберкулезные препараты, тетрациклины и β-лактамные антибиотики, проявляют противоопухолевую активность. Было показано, что бедаквилин, антибиотик, одобренный FDA для лечения туберкулеза легких, подавляет развитие и размножение стволовых раковых клеток, полученных из MCF7, а также снижает потребление кислорода митохондриями. Перспективы бедаквилина как химиотерапевтического варианта лечения рака обусловлены его способностью воздействовать на митохондриальную АТФ-синтазу, что может привести к истощению м-АТФ и нарушению работы митохондрий в раковых клетках. Однако для подтверждения этой гипотезы необходимы дальнейшие исследования [ 122 , 123 , 124 ].
Тетрациклины, такие как тигециклин и доксициклин, могут препятствовать распространению рака, целенаправленно воздействуя на систему окислительного митохондриального метаболизма. Воздействуя на такие пути, как опосредованный AMPK mTOR, WNT/b-катенин и PI3K/AKT, они вызывают окислительный стресс, аутофагию, остановку клеточного цикла и, в конечном итоге, апоптоз в раковых клетках, подавляя пролиферацию клеток, миграцию, инвазию и ангиогенез [ 78 , 125 , 126 ].
Клофоктол, медицинский препарат, используемый во Франции и Италии для лечения инфекций верхних дыхательных путей, обладает способностью ингибировать трансляцию белков в клетках млекопитающих, что указывает на его потенциальную полезность в области терапии рака. Клофоктол стимулирует стресс эндоплазматического ретикулума (ЭР) посредством активации пути ответа на развернутый белок (UPR), что приводит к остановке клеточного цикла в фазе G1 в раковых клетках. Учитывая, что многие раковые клетки демонстрируют повышенные уровни стресса ЭР, дополнительное усиление стресса ЭР может вызвать чрезмерные реакции на стресс, что приводит к остановке клеточного цикла или гибели клеток [ 127 , 128 ].
Антрациклины (AC), такие как доксорубицин, даунорубицин, эпирубицин и идарубицин, интеркалируют между парами оснований ДНК, образуя тройной комплекс с ДНК и топоизомеразой II, который ингибирует синтез ДНК и РНК в активно размножающихся раковых клетках. Схемы химиотерапии, содержащие доксорубицин, включая FAC (5-фторурацил, AC), TAC (таксотер, AC) и AC (адриамицин, циклофосфамид), оказались эффективными при лечении рака молочной железы. Миоцет, непегилированная липосомальная форма доксорубицина, лицензирована для лечения метастатического рака молочной железы в Европе и Канаде при использовании с циклофосфамидом [ 129 , 130 , 131 ].
Широкоспектральный тетрациклиновый антибиотик миноциклин продемонстрировал эффективность в лечении нескольких форм рака. Остановка клеточного цикла и подавление циклинов A, B и E являются механизмами, посредством которых он подавляет пролиферацию клеток рака яичников. Одновременное введение миноциклина и целекоксиба при раке молочной железы вызывает снижение пролиферации опухолевых клеток, плотности микрососудов и синтеза матриксной металлопротеиназы и VEGF. Активация аутофагии является механизмом, посредством которого миноциклин подавляет пролиферацию клеток глиомы. Текущие клинические испытания оценивают его способность улучшать результаты лечения онкологических больных путем смягчения побочных эффектов химиотерапии [ 132 , 133 ].
Тетрациклиновый антибиотик широкого спектра действия тигециклин эффективен против мультирезистентных бактерий и обладает противораковыми свойствами, включая ингибирование глиом, миелоидного лейкоза, немелкоклеточного рака легких и ретинобластомного транскрипционного корепрессора 1 рака молочной железы. Текущие испытания фазы I изучают использование тигециклина для лечения острого миелоидного лейкоза [ 126 , 134 , 135 ].
Фторхинолоны, включая ципрофлоксацин, моксифлоксацин, левофлоксацин, эноксацин и флероксацин, нарушают синтез ДНК, ингибируя бактериальную гиразу и демонстрируя сильные противораковые свойства. Например, было показано, что ципрофлоксацин ингибирует лейкемию, остеобластому, остеосаркому, рак толстой кишки, мочевого пузыря и простаты. Эноксацин модулирует выработку miRNA, особенно при раке, подчеркивая потенциал фторхинолонов как противораковых препаратов [ 136 , 137 ].
2.1.7. Перепрофилирование противомалярийных препаратов для лечения рака
Хлорохин, артесунат и мефлохин, изначально разработанные для лечения малярии, показали эффективность против различных заболеваний, включая рак. Хлорохин подавляет аутофагию, замедляет развитие опухоли в ксенотрансплантатах глиобластомы и улучшает общий результат при использовании с химиотерапевтическими препаратами. Артесунат индуцирует выработку ROS и апоптоз при Т-клеточной лейкемии и замедляет рост опухоли и ангиогенез при саркоме Капоши [ 138 ].
Мефлохин повышает эффективность других терапевтических средств при лечении нескольких типов рака, включая рак молочной железы, лейкемию, рак желудка, шейки матки и толстой кишки, за счет снижения экспрессии P-gp, блокирования деления клеток и нарушения лизосом посредством продукции ROS [ 139 , 140 ].
2.1.8. Перепрофилирование антипсихотических препаратов для лечения рака
Было показано, что антипсихотические препараты обладают противораковыми свойствами, влияя на биохимические пути, которые приводят к гибели опухолевых клеток. Галоперидол и пенфлуридол, антипсихотики на основе гидроксипиперидина, подавляют активность DRD2, способствуя стрессу ER и подавляя пролиферацию клеток рака поджелудочной железы с минимальной токсичностью. Пенфлуридол стимулирует аутофагию и гибель злокачественных клеток поджелудочной железы и оказывает синергическое действие в сочетании с гемцитабином. Пенфлуридол специфически воздействует на сайт связывания JAK2 в PRLR, тем самым блокируя сигнальные пути JAK2–STAT3 и ERK/AKT. Это действие эффективно подавляет пролиферацию клеток рака поджелудочной железы [ 141 , 142 , 143 ].
2.1.9. Перепрофилирование НПВП для лечения рака
Хроническое воспаление связано с риском рака, при этом воспалительные медиаторы, такие как факторы роста, хемокины и цитокины, способствуют выживанию и пролиферации раковых клеток. НПВП, такие как месалазин, сулиндак, пироксикам и ибупрофен, продемонстрировали потенциал в снижении роста опухоли и рецидива рака. Было обнаружено, что диклофенак замедляет рост опухоли поджелудочной железы, в то время как селективный ингибитор ЦОГ-2, целекоксиб, подавляет пролиферацию клеток рака молочной железы и образование опухоли. Корреляция между использованием НПВП и более медленным развитием рака предполагает потенциальные возможности повторного использования [ 144 , 145 ].
2.1.10. Перепрофилирование противоревматических препаратов, изменяющих течение заболевания (БПВП), для лечения рака
Ауранофин, модифицирующий заболевание противоревматический препарат (БПВП), когда-то использовался для лечения ревматоидного артрита путем подавления воспаления и стимуляции клеточно-опосредованного иммунитета. Однако было обнаружено, что он менее эффективен, чем другие БПВП, такие как метотрексат, и его использование сократилось из-за его побочных эффектов, включая желудочно-кишечные жалобы, раздражения кожи и язвы полости рта. Однако у него есть потенциал для новых применений в лечении некоторых злокачественных новообразований. Ауранофин эффективен против раковых клеток посредством двух механизмов: ингибирования млекопитающих TrxR (mTrxR) и воздействия на систему UPS (Understanding the Unstable Cells). Эти механизмы вызывают апоптоз, что указывает на то, что ауранофин больше не может быть предпочтительным лекарством для лечения ревматоидного артрита [ 146 , 147 ]. Не только золотой комплекс, ауранофин, показавший многообещающие противораковые эффекты, но и другие комплексы металлов с клинически одобренными препаратами, имеющими различные терапевтические применения, также привели к перепозиционированию таких комплексов для терапии рака. Примерами являются метформин-декаванадат, ванадий-бисфосфонаты, комплексы ванадила(IV) с нестероидными противовоспалительными препаратами, а также комплексы оксидованадия(IV) на основе цетиризина и имидазола [ 147 , 148 ].
2.1.11. Перепрофилирование противоэпилептических препаратов для лечения рака
Окскарбазепин — это широко используемый фармацевтический препарат, специально разработанный для лечения эпилепсии. Многочисленные доклинические исследования предоставили доказательства его противораковых возможностей. Одно исследование показало, что окскарбазепин приводит к остановке клеточного цикла, особенно во время митоза. Дополнительные исследования предполагают, что он действует как ингибитор HDAC, тем самым подавляя последующий путь PI3K-Akt-mTOR. Конечным результатом этого ингибирования является предотвращение роста и миграции клеток. В конечном итоге это подавление препятствует проявлению mTOR и белков Bax и Bcl-2, способствуя экспрессии каспазы-3 и каспазы-9, что приводит к апоптозу и аутофагии [ 149 , 150 ].
Препарат лакосамид относится к третьему поколению противоэпилептических препаратов, которые улучшают замедленную дезактивацию потенциалзависимых Na + каналы. Он используется в качестве дополнительного лечения, поскольку он способен снижать частоту приступов, не влияя существенно на настроение [ 150 ]. Было обнаружено, что лакосамид также ингибирует HDAC во время обработки. Эта активность может указывать на необходимость проведения исследования его противораковых свойств. Более того, этот процесс был предложен в качестве возможного обоснования ингибирования миграции клеточного цикла в клетках глиомы, которое может быть вызвано повышением уровней miR-195-5p [ 151 ]. В том же исследовании было высказано предположение, что лакосамид может подавлять клеточную пролиферацию, препятствовать миграции и инвазии клеток и стимулировать апоптотические процессы, изменяя выработку других микроРНК, таких как miR-107. Исследовательская группа представила доказательства, указывающие на то, что фосфорилирование белка-медиатора коллапсина (CRMP2) является сильным индикатором пролиферации клеток глиобластомы [ 151 , 152 ].
Для того чтобы изучить влияние фосфорилирования CRMP2 на S522 на рост опухоли, исследователи использовали ингибитор фосфорилирования CRMP2 (S)-лакосамид. Было показано, что ингибирование фосфорилирования CRMP2 с помощью (S)-лакосамида снижает пролиферацию клеток глиобластомы во всех клеточных линиях глиобластомы. Кроме того, они предоставили доказательства того, что (S)-лакосамид подавляет рост глиобластомы в моделях живых животных [ 153 , 154 ].
Ламотриджин — еще один противоэпилептический препарат, который подавляет транспорт соли. Помимо первичной блокировки потенциалзависимого Na + каналы, он также ингибирует кальциевые каналы N-, L- и P-типа и, в меньшей степени, рецепторы 5-HT3. За счет снижения синтеза глутамата эти эффекты повышают стабильность нейрональных мембран. Подобно лакосамиду, ламотриджин является потенциальным вспомогательным препаратом для пациентов с диагностированными опухолями мозга. Опубликованные исследования показывают, что его сочетание с вальпроевой кислотой может улучшить лечение рефрактерной эпилепсии за счет использования синергии [ 155 , 156 ].
2.1.12. Перепрофилирование анестетиков для лечения рака
Кетамин в основном используется для индукции и поддержания анестезии из-за его антагонистического действия на рецептор N-метил-D-аспартата (NMDA). Он вызывает диссоциативную анестезию, описываемую как состояние, подобное трансу, а также может вызывать амнезию и облегчать боль. Поэтому кетамин рекомендуется онкологическим больным для минимизации боли. Кроме того, первоначальные исследования показали, что введение кетамина в определенные клетки приводит к прекращению клеточного цикла и подавлению деления клеток, что предполагает возможное будущее использование кетамина для профилактики прогрессирования рака. Чжоу и др. [ 157 ] показали, что введение кетамина способствует апоптозу в клетках рака легких за счет увеличения экспрессии CD69, маркера, связанного с активацией лейкоцитов и естественных клеток-киллеров (NK). Кетамин проявляет свои противораковые свойства при раке яичников, специфически снижая экспрессию РНК PVT1. Более того, терапия кетамином снизила взаимодействие между PVT1 и усилителем гистонметилтрансферазы гомолога zeste 2. Вышеупомянутая связь приводит к увеличению экспрессии P57, ингибитора клеточного цикла, который впоследствии препятствует продвижению клеточного цикла в злокачественных клетках. В клетках рака молочной железы и гепатоцеллюлярных карциномах введение кетамина может ингибировать рост клеток и вызывать ферроптоз, а также апоптоз, путем специфического ингибирования глутатионпероксидазы 4 [ 52 ].
Пропофол — это быстродействующий, эффективный внутривенный анестетик с анальгетическими, снотворными и седативными свойствами. Он вызывает центральный ингибирующий нейротрансмиттерный ответ путем активации центральных рецепторов ГАМК, подобно барбитуратам и бензодиазепинам. Было обнаружено, что пропофол обладает противовоспалительными свойствами и может усиливать иммунологический ответ у пожилых людей. Исследования показывают, что пропофол может снижать цитотоксическую активность NK-клеток у людей с желудочно-кишечными заболеваниями, одновременно повышая их эффективность у пациентов с анестезией пропофолом. Пропофол также изучался на предмет его антипролиферативного действия на различные раковые клетки, подавляя репликацию клеток и стимулируя пути каспазы и MAPK. Он может вызывать апоптоз при плоскоклеточном раке полости рта, устойчивом к 5-фторурацилу, и обращать вспять устойчивость OSCC к 5-фторунипролактону [ 158 ].
2.2. Перепрофилирование с типоспецифической противораковой активностью
2.2.1. Перепрофилирование лекарств для лечения рака предстательной железы (РПЖ)
- Антидислипидемические препараты
Тяжесть рака предстательной железы (РПЖ) связана с уровнем циркулирующих андрогенов, в первую очередь происходящих из холестерина. Клетки РПЖ зависят от эндогенной продукции холестерина, что делает пациентов с высоким уровнем сывороточного холестерина более восприимчивыми к РПЖ. Статины, которые ингибируют ГМГ-КоА-редуктазу, блокируют синтез холестерина и продукцию андрогенов, улучшая прогноз, уменьшая объем опухоли и снижая уровень ПСА. Статины, такие как аторвастатин, продемонстрировали потенциал в лечении РПЖ, как в качестве монотерапии, так и в комбинации [ 159 , 160 ].
- Антиаритмические препараты
Натрий-калиевый насос ингибируется сердечными гликозидами, включая дигоксин и уабаин, что приводит к накоплению внутриклеточного кальция и гибели клеток PC. Кроме того, эти препараты стимулируют остановку клеточного цикла и аутофагию. Дигоксин подавляет активность топоизомеразы II и снижает уровень ПСА в крови, в то время как уабаин повышает восприимчивость клеток PC к апоптозу, блокируя выработку сурвивина и STAT3. Уабаин также демонстрирует противораковую цитотоксичность при резистентном к кастрации PC [ 160 , 161 ].
Таблица 1. Перепрофилированные препараты для лечения рака с указанием их химической структуры, новых показаний, старых и новых мишеней, а также статуса разработки (см. прикрепленный файл).
- Противовоспалительные препараты
Индометацин, неселективный ингибитор ЦОГ, подавляет ангиогенез и рост раковых клеток различными путями. Диклофенак подавляет ЦОГ, синтез простагландинов и экспрессию семейства генов MYC, нарушая метаболизм глюкозы в клетках ПК. Аспирин подавляет ЦОГ, простагландины и NF-κB, что делает его потенциальным кандидатом для лечения ПК, особенно в сочетании со статинами [ 179 ].
- Антидепрессанты
Сертралин, селективный ингибитор обратного захвата серотонина, снижает пролиферацию клеток PC и индуцирует апоптоз посредством митохондриальной дисфункции и продукции ROS. Сертралин также подавляет опухолеобразование, ангиогенез и метастазирование, нарушая жизнеспособность стволовых клеток PC путем модуляции гомеостаза железа. Смягчение стресса имеет решающее значение для успешного лечения рака, и сертралин продемонстрировал потенциал для снижения жизнеспособности клеток PC, ингибирования пролиферации клеток и усиления аутофагии [ 180 ].
- Бета-блокаторы
Бета-блокаторы — это кардиопротекторные препараты с потенциальными противораковыми свойствами. Они ингибируют β-адренорецепторы, участвующие в канцерогенезе, ангиогенезе и метастазах опухолей. Бета-блокаторы показали многообещающие результаты в снижении пролиферации раковых клеток, миграции и роста опухолей, особенно при нейроэндокринном раке простаты (NEPCA). Пропранолол нарушает путь CREB1-EZH2-TSP1, подавляя маркеры NE и способствуя развитию ксенотрансплантата из клеток NEPCA [ 181 ].
- Другие группы
Гепарин, антикоагулянт, показал потенциал как противовоспалительное и антиметастатическое средство при лечении рака. Он подавляет экспрессию цитокинов, молекул адгезии и ангиогенных факторов, нарушая каскад коагуляции, опосредованный опухолью. Низкомолекулярный гепарин (НМГ) проявляет антиангиогенные и антиметастатические эффекты, значительно снижая метастазы в мышиной модели CRPCA [ 182 ].
Бисфосфонатный препарат золедроновая кислота блокирует резорбцию костей, подавляя активность остеокластов. Поэтому он используется при лечении остеопороза. Терапевтическое применение этого перепрофилированного препарата при лечении рака предстательной железы получило одобрение. Кори и коллеги показали, что анти-ПК свойства золедроновой кислоты in vitro вызывают остановку G1, замедление пролиферации клеток и смерть, а in vivo — снижение способности к метастазированию. Цинк-азитромицин эффективно уменьшает проблемы, связанные со скелетом, у пациентов с ПК с метастазами в костях, в то же время подавляя рост остеобластических и остеолитических метастазов при ПК. Целекоксиб, ингибитор ЦОГ-2, в сочетании с заметакселом не улучшил показатели выживаемости у пациентов с ПК на поздней стадии. Однако доцетаксел и заэтаксел значительно улучшили прогноз у пациентов с ПК. Мифепристон, мощный антипрогестерон, показал противораковые свойства в андроген-чувствительном и андроген-нечувствительном PC. Он подавляет пролиферацию опухоли, подавляя сверхэкспрессированные рецепторы клеточной поверхности в клетках CRPC. Рапамицин, антирестенозный препарат и иммунодепрессант для трансплантации почек, был перепрофилирован для лечения рака путем связывания с доменом FRB mTOR, ингибируя mTORC1 [ 183 , 184 ].
2.2.2. Перепрофилированные лекарственные средства в лечении рака желудка (РЖ)
- Антидепрессанты
Флуоксетин — селективный ингибитор обратного захвата серотонина (СИОЗС), используемый для лечения депрессии, тревожности и посттравматического стрессового расстройства. Он показал противораковый потенциал в раковых клетках, вызывая апоптоз и нарушение клеточного цикла. Флуоксетин подавляет пролиферацию клеток в клетках AGS GC и вызывает апоптоз, который частично подавляется ингибированием маркера стресса эндоплазматического ретикулума (CHOP). Он также усиливает апоптоз и образование аутофагосом в клетках AGS.
Сертралин, СИОЗС, показал противоопухолевую активность в легких, простате, груди, меланоме и остром миелоидном лейкозе. Он вызывает апоптоз и остановку клеточного цикла в резистентных клетках GC, что приводит к росту, устойчивости к терапии, ангиогенезу и метастатическому потенциалу. Сертралин и его производные могут быть повторно использованы в качестве химиосенсибилизаторов для резистентных GC.
Пароксетин, СИОЗС, также обладает противораковыми свойствами, вызывая апоптоз и подавляя пролиферацию раковых клеток в толстой кишке, гепатоцеллюлярной карциноме, остеосаркоме и лимфоме. Его цитотоксичность в клетках AGS усиливается за счет усиления повреждения ДНК и снижения репарации ДНК. Однако он не способен вызывать апоптоз или повреждение ДНК в клетках MKN-45. Сочетание пароксетина с химиотерапией или противораковыми средствами может усилить лечение GC [ 185 ].
- Противоэпилептическое
Вальпроевая кислота (VPA) — жирная кислота с противосудорожными свойствами, которая, как было показано, обладает противораковыми свойствами при различных видах рака. VPA индуцирует апоптоз и подавляет пролиферацию клеток в клетках AGS GC, ингибируя сигнальный путь HDAC1/PTEN/Akt, который влияет на пролиферацию клеток, дифференцировку и иммунитет. Она также усиливает экспрессию Beclin1, супрессора опухолей, и ингибирует экспрессию Bcl-2. Однако высокая экспрессия HDAC1 и сниженная экспрессия PTEN в клетках MKN-74 GC делают их устойчивыми к лечению VPA. In vivo VPA ингибирует рост клеток GC посредством апоптоза и аутофагии и увеличивает экспрессию сурвивина, белка, необходимого для деления клеток. В отдельном исследовании VPA показала повышенный апоптотический индекс и уменьшение объема опухоли. Однако рандомизированное исследование фазы II показало, что VPA не обеспечивает преимущества в плане выживаемости по сравнению с одним паклитакселом в терапии второй или третьей линии при распространенном раке желудка [ 185 , 186 ].
- Антипсихотические
Тиоридазин и рисперидон являются антипсихотическими соединениями, которые используются для лечения острой мании, биполярного расстройства и шизофрении в психиатрической области. При глиобластоме, злокачественных новообразованиях легких и толстой кишки тиоридазин демонстрирует противоопухолевые свойства. Тиоридазин индуцирует апоптоз каспазозависимым образом и подавляет способность к образованию колоний и фрагментацию ядер в клетках NCI-N87 и AGS GC, тем самым оказывая цитотоксическое действие таким образом, что снижается количество предшественников каспазы-9, каспазы-8 и каспазы-3. Этот препарат обладает способностью ингибировать рост опухолей in vivo. Рисперидон предотвращает пролиферацию клеток KATO-III GC, повышая уровень ROS и вызывая апоптоз.
Кроме того, этот препарат подавляет рост опухолей in vivo. В популяционном когортном исследовании были продемонстрированы противораковые эффекты рисперидона. Пациенты, которые использовали рисперидон, имели более низкий риск GC по сравнению с теми, кто его не использовал [ 187 , 188 ].
- Агенты, хелатирующие железо
Деферазирокс, тридентатный хелатор железа, как было показано, обладает противоопухолевой активностью при различных злокачественных новообразованиях, включая рак поджелудочной железы и молочной железы, мантийноклеточную лимфому и лимфому. Он подавляет пролиферацию клеток AGS, MKN-28, SNU-484 и SNU-638 GC, вызывает апоптоз и повышает регуляцию нижестоящего регулируемого гена N-myc 1, ингибируя метастазирование. Он также снижает экспрессию фосфо-mTOR и c-myc, что позволяет предположить, что деферазирокс может усиливать противоопухолевый эффект цисплатина при GC [ 185 , 189 ].
2.2.3. Перепрофилированные лекарственные средства в лечении злокачественных новообразований крови
Талидомид был разработан в 1950-х годах, изначально как седативное средство, и использовался для облегчения утренней тошноты у беременных женщин. После его появления талидомид был отозван с рынка из-за его способности вызывать серьезные врожденные аномалии. По оценкам, минимум 10 000 новорожденных родились с аномалиями конечностей и других частей тела в более чем 46 странах в течение этого периода. В течение следующих десятилетий ученые настойчиво исследовали лекарственное применение талидомида [ 190 , 191 ].
Лаборатория Джуды Фолкмана предоставила доказательства того, что талидомид значительно снижает образование новых кровеносных сосудов. После тщательной оценки у пациентов с рефрактерной множественной миеломой лекарство продемонстрировало способность вызывать долгосрочные эффекты, блокируя TNF-α. Талидомид получил одобрение FDA в 2006 году в качестве терапевтического варианта для множественной миеломы при применении в сочетании с дексаметазоном [ 192 , 193 ].
Довольно типично, что препараты для лечения рака повторно используются в рамках того же подтипа заболевания, для которого они изначально были предназначены. Например, иматиниб мезилат был первоначально одобрен для лечения хронического миелоидного лейкоза. Тем не менее, иматиниб продемонстрировал перекрестную реактивность и способность подавлять киназу KIT, поскольку он действует как ингибитор киназы ABL. Выявление мутаций, которые активируют тирозинкиназу KIT как генетический фактор, способствующий желудочно-кишечным стромальным опухолям (GIST), предполагает, что иматиниб следует оценить на предмет его эффективности при лечении GIST. Понятие возможного показания было изучено с помощью доклинических анализов, которые подтвердили, что иматиниб действительно вызывал гибель клеток GIST. Это явление было теоретически связано с подавлением киназы KIT. Терапевтическое использование иматиниба при GIST было одобрено на основании этих исследований [ 193 ]. Текущим показанием к применению иматиниба является лечение некоторых злокачественных заболеваний крови, таких как острый лимфобластный лейкоз, хронический эозинофильный лейкоз и миелодиспластические/миелопролиферативные новообразования. Кроме того, он получил одобрение для лечения системного макроцитоза и дерматофибросаркомы, вызванных аллергической реакцией [ 194 , 195 ].
Дазатиниб, первоначально одобренный для лечения хронического миелоидного лейкоза, впоследствии был адаптирован для лечения лиц с острым лимфобластным лейкозом с положительной филадельфийской хромосомой, у которых наблюдалась резистентность или непереносимость предыдущего фармацевтического лечения, похожего на иматиниб. Дазатиниб — это пероральный ингибитор тирозинкиназы, который активно изучается в клинических исследованиях для лечения глиобластомы. Кроме того, он использовался для лечения метастазов в мозг, вызванных раком молочной железы, с использованием сетевых методов, которые используют реконструкцию сетей, специфичных для заболевания, для точного определения важных целей [ 196 , 197 ].
2.2.4. Перепрофилированные лекарства в лечении рака молочной железы
Фторурацил (5-FU) — гетероциклическая ароматическая молекула, имеющая рибиноидную структуру, похожую на пиридиновое кольцо, присутствующее в ДНК и РНК. Точнее, гомолог урацила заменяет водород на фтор в положении C-5. Терапевтическое использование 5-FU для пациентов с церебральным параличом было одобрено FDA США. Базальноклеточная карцинома обычно лечится 5-FU.
Существует несколько признанных методов, с помощью которых он оказывает свое противораковое действие, включая стимуляцию апоптоза и подавление роста раковых клеток (например, путь Ras/ERK). Соединение 5-FU проявило апоптотические эффекты и снизило экспрессию гена H-ras в исследованиях in vitro с использованием линий клеток MDA-MB-231 и Tumor2 [ 198 ].
Более того, подавляется путь Ras/ERK, не вызывая антипролиферативных действий. Кроме того, 5-FU снижает экспрессию гена Rho-A, тем самым снижая апоптоз и метастазирование. 5-FU заметно снизил экспрессию белка Rac1 в клетках Tumor2 и MDA-MB-231, который играет решающую роль в движении клеток, инвазии и устойчивости к клеточной смерти. 5-FU снизил экспрессию гена p53 в Tumor2. Активация NF-κB обычно обнаруживается в клетках рака молочной железы. Исследование показало, что пролиферация и выживаемость раковых клеток, а также экспрессия гена NF-κB были снижены после лечения 5-FU. Исследование показало, что 5-FU снизил экспрессию белка в клеточной линии tumor2 по сравнению с его эквивалентами. Многочисленные результаты подтверждают представление о том, что активация NF-κB снижает лекарственную устойчивость к 5-FU в линиях раковых клеток человека. Это дает явное превосходство над доступными в настоящее время лекарствами, которые находятся на вершине лекарственной устойчивости. Дополнительные исследования предоставляют дополнительные доказательства, подтверждающие предыдущие исследования, демонстрируя, что терапевтическая эффективность 5-FU была повышена в результате снижения экспрессии NF-κB. Сочетание 5-FU с другими методами лечения повышает вероятность значительного ответа в условиях лекарственно-устойчивых видов рака [ 199 ].
Нитроксолин (NTX) — антибиотик, который широко используется в странах Азии, Европы и Африки для эффективного лечения инфекций мочевыводящих путей. Он химически известен как 5-нитро-8-гидроксихинолин. В настоящее время нитроксолин пользуется значительной популярностью из-за своих мощных противораковых свойств. Антиангиогенная активность нитроксолина была первой противораковой активностью, которая была задокументирована при раке мочевого пузыря у человека. NTX продемонстрировал перспективную противоопухолевую активность против различных злокачественных новообразований, включая лимфому, глиому, лейкемию, рак молочной железы, мочевого пузыря, поджелудочной железы и яичников [ 199 ]. Это особенно примечательно. Сообщалось, что NTX уменьшает объем опухолей в модели ксенотрансплантатов BC на 60% и подавляет развитие рака мочевого пузыря в ортотопической мышиной модели. В моделях рака молочной железы у мышей MMTV-PyMT и LPB фибросаркомы нитроксолин значительно ингибировал развитие опухоли, ангиогенез и метастазирование in vivo. Катепсин B ингибируется NTX, уровень которого повышен у пациентов с BC. Ингибирование катепсина B приводит к снижению деградации ECM и последующей инвазии в моделях 2D и 3D опухолей [ 200 ].
NTX значительно снижает рост опухоли и метастазирование, взаимодействуя с MetAP2, SIRT1 и Cat B in vivo, тем самым подавляя развитие эндотелиальных клеточных трубок. Исследование показало, что NTX устраняет такие признаки рака, как инвазия, ангиогенез и метастазирование в моделях in vivo, независимо от пути введения. Это превосходный препарат против рака молочной железы по сравнению с текущими схемами из-за его исключительного фармакокинетического профиля и отсутствия системной токсичности [ 157 ].
2.2.5. Перепрофилированные лекарства в лечении рака толстой кишки
- Антигипертензивные и антиаритмические препараты
Препараты ИАПФ и БРА широко используются и обеспечивают значительные терапевтические преимущества для пациентов, проходящих лечение от многих заболеваний, включая гипертонию и сердечную недостаточность. Исследование in vivo показало, что как ИАПФ, так и БРА эффективно подавляли колоректальный рак (КРР), вызванный колитом, у тучных мышей за счет снижения хронического воспаления и окислительного стресса. В независимом исследовании, проведенном Кедикой и соавторами, у лиц, у которых был один или несколько аденоматозных полипов, подтвержденных гистологическим анализом при первой колоноскопии, и которым был назначен лизиноприл, противоопухолевый химиотерапевтический препарат, наблюдалось снижение вероятности приобретения подобных полипов на 41% в течение следующих 3–5 лет. Кроме того, исследования показали, что совместное использование ИАПФ/БРА и бета-блокаторов приводило к более высоким показателям выживаемости, снижению госпитализации и замедлению прогрессирования опухоли при запущенном колоректальном раке [ 201 , 202 , 203 ].
Бета-блокаторы — это фармакологические средства, классифицируемые как антиаритмические препараты II класса, в основном предназначенные для лечения сердечно-сосудистых заболеваний и ряда других синдромов. Исследование показало, что небиволол специфически подавляет митохондриальное дыхание в клеточной линии рака толстой кишки HCT-116. Это было достигнуто путем угнетения функции комплекса I в дыхательной цепи и ингибирования пролиферации клеток рака толстой кишки. Такие доказательства подразумевают, что этот препарат может быть повторно использован для лечения рака толстой кишки [ 31 , 201 , 204 ].
- Противоглистное
Для ряда линий клеток CRC, включая HCT-116, RKO, HT-29, HT-8 и SW626, мебендазол демонстрирует цитотоксическое действие. Нигрен и Ларссон наблюдали, что мебендазол успешно вызывал частичную регрессию метастатических поражений у пациента с рефрактерным метастатическим CRC. Отдельное исследование показало, что комбинация мебендазола и сулиндака (НПВП) уменьшала количество и размер микроаденом кишечника у мышей с конституционной мутацией в гене Adenomatous polyposis coli (APC) путем блокирования путей MYC и COX-2, ангиогенеза и высвобождения протуморогенных цитокинов [ 62 , 70 , 172 ].
Производное салициламида, никлозамид, модулирует несколько сигнальных путей и диссоциирует окислительное фосфорилирование. Как в лабораторных, так и в животных исследованиях никлозамид подавлял каскад Wnt/β-катенина, который аномально активен в 80% спорадических CRC. Возможно, через стимуляцию аутофагии, эта понижающая регуляция привела к снижению пролиферации в нескольких линиях клеток CRC человека, включая HCT-116, Caco2 и HT-29. Более того, недавнее исследование показало, что комбинация никлозамида и метформина может эффективно снижать Wnt и YAP, тем самым кооперативно ингибируя APC-мутантный CRC [ 162 , 163 , 164 ].
Сиролимус, часто известный как рапамицин, является одобренным FDA ингибитором пути mTOR, используемым для предотвращения отторжения после трансплантации почки. Синергетическое ингибирование роста опухоли толстой кишки комбинацией сиролимуса и метформина было продемонстрировано Муссином и соавторами как в условиях in vitro, так и in vivo. В своем исследовании он и его коллеги представили доказательства того, что ингибиторы mTOR вызывают гибель клеток рака толстой кишки, способствуя дефосфорилированию 4EBP1 через CHOP-зависимый DR5. Этот процесс в конечном итоге приводит к снижению роста опухоли, ангиогенеза и инвазии. Было показано, что сиролимус подавляет активность mTOR, что, в свою очередь, снижает миграцию и инвазию клеток CRC, тем самым ингибируя ЭПТ, вызванный делецией FBXW7 [ 165 , 166 , 167 ].
2.2.6. Перепрофилированные лекарства в лечении гепатоцеллюлярной карциномы (ГЦК)
Пимозид, антипсихотический препарат, потенциально может подавлять рост линий клеток гепатоцеллюлярной карциномы (ГЦК) в лабораторных условиях, вызывая апоптоз во время фазы G0/G1. Более того, пимозид оказывал ингибирующее действие на стволовые клетки ГЦК, в частности, нацеливаясь на популяцию клеток, положительных по CD133. Активность анализа люциферазы пимозида была направлена на экспрессию STAT3, что привело к снижению уровней транскрипции нижестоящих онкогенов, участвующих в сигнальной активности STAT3. Дальнейшая проверка противоракового эффекта пимозида была проведена in vivo с использованием голых грызунов [ 142 , 205 , 206 ].
Амиодарон, антиаритмический препарат класса III и агрессивный ингибитор mTOR, как было показано, снижает развитие опухолей печени, стимулируя активность аутофагии как в мышиной модели ксенотрансплантата, так и в крысиной ортотропной модели. Более того, комплексное обследование 32 625 участников случай-контроль из Национальной программы медицинского страхования Тайваня показало, что постоянное долгосрочное использование амиодарона значительно снижает заболеваемость ГЦК. Амиодарон, перепрофилированный препарат, обладает противораковыми свойствами посредством стимуляции активности аутофагии, что может подавлять развитие опухолей печени и предотвращать возникновение ГЦК [ 207 , 208 ].
Ланатозид C — это эндогенное соединение, полученное из наперстянки шерстистой, известное своими антиаритмическими свойствами. Способность ланатозида C модулировать ГЦК как в лабораторных условиях, так и в живых организмах была продемонстрирована путем включения стратегии системной биологии репозиционирования, что привело к значительному снижению пролиферации опухоли. Молекулярно-механистический анализ показал, что ланатозид C может вызывать гибель клеток, способствуя истощению потенциала митохондриальной мембраны. Таким образом, происходит активация апоптотических маркеров. Благодаря подавлению фосфорилирования Thr505 для протеинкиназы дельта (PKCd) ланатозид C обратил вспять вызванную ланатозидом Ce потерю и гибель митохондриального мембранного потенциала, что подтверждает его молекулярный механизм, который включает путь AKT/mTOR посредством контроля активации PKCd [ 207 , 209 ].
Одобренное FDA лекарство от пневмоцистной пневмонии, атовакуон, значительно подавило рост HCC, остановив S-фазу клеточного цикла и усилив как внутренние, так и внешние апоптотические пути, которые были связаны с повышенной экспрессией p53 и p21. Было показано, что посредством индукции двухцепочечных разрывов ДНК атовакуон подавляет рост клеток гепатомы, вызывая длительную активацию мутанта атаксии-телеангиэктазии и его нижестоящих компонентов, включая контрольную точку клеточного цикла киназу-2 и H2AX. Кроме того, атовакуон подавлял пролиферацию клеток и ангиогенез in vivo, способствовал апоптозу и продлевал период выживания мышей с опухолями, все это без каких-либо заметных негативных последствий [ 210 , 211 ].
Таблица 2. Перепрофилированные препараты для лечения определенных типов рака с указанием их химической структуры, старых и новых мишеней и статуса разработки (см. прикрепленный файл).
2.3. Перепрофилирование с направленной на механизм противораковой активностью
2.3.1. Перепрофилированные лекарства для воздействия на митохондриальный энергетический метаболизм при раке
- Антидиабетические
Другой примечательной характеристикой метформина является его способность специфически воздействовать на окислительное фосфорилирование. Эмпирические данные показывают, что метформин может проявлять свои антидиабетические свойства, специфически воздействуя на комплекс I митохондриальной дыхательной цепи. Действительно, недавние исследования показали, что метформин притупляет функцию комплекса I в широком спектре видов рака [ 60 , 168 ].
Более того, метформин, как полагают, ингибирует комплекс I, который отвечает за снижение потребления кислорода в различных моделях рака. Метформин также снижает выработку АТФ в различных злокачественных новообразованиях. В некоторых случаях уровни экспрессии транскриптов комплекса I были изменены, а соотношение НАДН/НАД было снижено. Недавние исследования показывают, что метаболическая среда опухоли является определяющим фактором в антипролиферативном эффекте метформина, поскольку она имеет потенциал значительно изменять чувствительность к препарату [ 60 , 168 ]. В целом, метформин в первую очередь влияет на прогрессирование рака, увеличивая скорость гибели клеток и уменьшая пролиферацию опухолевых клеток. Было показано, что фенформин повышает радиочувствительность раковых клеток и подавляет экспрессию комплекса I и потребление кислорода при колоректальном раке. Было показано, что фенформин ингибирует рост опухоли в мышиных моделях рака с нарушением окислительного фосфорилирования. Более того, фенформин и оксаматный ингибитор лактатдегидрогеназы синергически снижают дыхание и выработку АТФ [ 169 , 170 , 217 ].
Аналогично, эта комбинация лекарств подавляет пролиферацию клеток и рост злокачественных новообразований. Канаглифозин, фармакологический препарат, используемый для лечения диабета, подавляет пролиферацию клеток комплекса I и карциномы при раке простаты и легких и проявляет синергическое воздействие при сочетании с лучевой и химиотерапией. Пиоглитазион при сочетании с ингибитором гликолиза 2-дезоксиглюкозой оказывает антипролиферативное действие, подавляет потребление кислорода и специфически влияет на митохондрии [ 171 , 174 , 218 , 219 ].
- Антимикробные
Действительно, неблагоприятные метаболические события (AM) могут вызывать нарушение работы митохондрий как в здоровых, так и в раковых клетках. Однако злокачественные клетки, которые быстро делятся и нуждаются в значительном энергетическом потреблении, особенно уязвимы для AM. Ниже представлены дополнительные исчерпывающие примеры противомикробных препаратов, которые подавляют рак путем изменения митохондриального аэробного метаболизма. Члены семейств тетрациклинов и хлорамфениколов часто используемых антибиотиков блокируют как митохондриальную, так и бактериальную трансляцию. Согласно ингибированию митохондриальной трансляции, эти антибиотики снижают активность комплексов окислительного фосфорилирования I, IV и V, которые состоят из компонентов, кодируемых митохондриями [ 174 , 175 , 176 ].
Первоначально разработанный для устранения аэробных бактерий, антибиотик бедаквилин специфически воздействует на митохондриальную и бактериальную АТФ-синтазу [ 123 ]. Противомалярийный препарат атовакуон действует как ингибитор окислительного фосфорилирования комплекса III. Ивермектин, терапия, которая особенно эффективна против ряда паразитов, подавляет активность комплекса I [ 215 , 216 ].
Пирвиниум памоат предотвращает активность митохондриального механизма НАДН-фумаратредуктазы, состоящего из комплекса I и II, который отвечает за лечение малярии и инфекций, вызываемых острицами [ 220 , 221 ].
Противогрибковый препарат широкого спектра действия итраконазол связывается с потенциал-зависимым митохондриальным белком анион-селективного канала 1 (VDAC1) и снижает синтез АТФ [ 222 , 223 , 224 ].
Кроме того, хинолоны, аминогликозиды, β-лактамы и оксазолидиноны являются дополнительными категориями антибактериальных веществ, которые вызывают нарушение митохондриальной активности в клетках млекопитающих. Тем не менее, влияние их антибактериальных свойств на аэробный метаболизм в раковых клетках не было тщательно исследовано [ 225 , 226 ].
2.3.2. Перепрофилированные препараты как индукторы ROS при раке
Тигециклин — антибиотик, одобренный FDA для лечения пневмонии, сложных инфекций и бактериальных инфекций с множественной лекарственной устойчивостью. Он подавляет синтез белка, что приводит к гибели бактерий. Тигециклин очень эффективен против рака, повышая уровень активных форм кислорода. Он подавляет митохондриальное дыхание, мембранный потенциал и уровень АТФ, вызывая гибель клеток. Он также повышает эффективность традиционного цисплатина против гепатоцеллюлярной карциномы человека. Кроме того, было успешно завершено клиническое исследование фазы I, оценивающее безопасность и биологическую эффективность внутривенных инфузий тигециклина при остром миелоидном лейкозе [ 177 , 227 ].
Левофлоксацин, антибиотик фторхинолонового ряда третьего поколения, также продемонстрировал потенциал для лечения рака. Он подавляет пролиферацию и апоптоз клеток рака легких, ингибируя функцию комплекса митохондриальной цепи переноса электронов и продукцию ROS. Он избирательно воздействует на клетки рака молочной железы и работает с 5-FU, ингибируя продукцию митохондрий [ 178 , 227 ].
Альбендазол — нетоксичный противопаразитарный препарат, который устраняет паразитов путем подавления синтеза АТФ и ограничения запасов гликогена. Было показано, что он вызывает окислительный стресс при лечении рака, запуская апоптоз и гибель клеток MCF-7. Это связано с пониженным уровнем глутатиона, обогащением окислительных биомаркеров и повышенной активностью антиоксидантных ферментов [ 173 , 228 ].
Пимозид, одобренный FDA антипсихотический препарат, был впервые идентифицирован как антагонист дофамина с активностью против меланомы в 1979 году. Он был испытан на раковых клетках, показав, что он подавляет раковые клетки, генерируя ROS. Однако клинические испытания, изучающие его противораковые эффекты, не проводились [ 141 , 205 , 213 , 214 ].
Таблица 3. Перепрофилированные препараты для лечения рака с направленным механизмом действия с их химической структурой, старыми и новыми показаниями и статусом разработки (см. прикрепленный файл).
- ВЫВОДЫ
Подход к лечению рака, известный как повторное использование лекарств, является многообещающим, поскольку он открывает окно возможностей для открытия новых лекарств и является развивающейся тенденцией в этой области. Во всем мире рак является одной из наиболее распространенных причин смертности, что привело к экономическим и общественным проблемам в области здравоохранения. Тем не менее, лечение рака сталкивается с многочисленными проблемами, включая развитие механизмов устойчивости опухолевых клеток к противораковым препаратам и снижение терапевтической эффективности существующих методов лечения. Это подчеркивает настоятельную необходимость в создании инновационных лекарств или стратегий борьбы с раком.
Перепрофилирование лекарств — это экономически эффективный и экономящий время метод увеличения числа клинически доступных лекарств для лечения рака, тем самым способствуя разработке более персонализированных методов лечения. Популярной в настоящее время темой в лечении рака является медицина точности, что является результатом гетерогенности, связанной с этим заболеванием.
Злокачественные новообразования человека — это отдельные заболевания, требующие отдельных вариантов и подходов к лечению. За последние два десятилетия был достигнут значительный прогресс в открытии новых фармацевтических препаратов для различных злокачественных заболеваний. Однако значительная часть онкологических больных в конечном итоге не поддается лечению из-за развития устойчивости к существующим препаратам, что является причиной раздражения ученых и врачей. Во многих странах отсутствуют финансовые возможности для покрытия растущих расходов на современное химиотерапевтическое лечение. Поэтому повторное использование лекарств рассматривается как весьма перспективный подход к выявлению новых противораковых методов лечения, которые являются как экономически эффективными, так и могут быть быстро разрешены для коммерциализации.
В настоящее время проводятся клинические испытания с повторно используемыми препаратами, которые показали многообещающую противораковую активность в доклинических исследованиях. Некоторые препараты были успешно повторно использованы и получили одобрение FDA для лечения злокачественных заболеваний человека, в то время как другие все еще находятся в стадии разработки. Фармакологический метаанализ препаратов, включая аспирин, статины и метформин, обнаружил значительную связь со снижением риска рака. Ожидается, что эти препараты будут развиваться дальше с клиническим одобрением для терапии рака.
Значимость повторного использования лекарственных препаратов как стратегии быстрой и экономически эффективной идентификации потенциальных противораковых средств в настоящее время все больше подтверждается растущим объемом доказательств.
Подводя итог, можно сказать, что повторное использование лекарств открывает существенные возможности в терапии рака, позволяя разрабатывать более экономически эффективные и ускоренные варианты лечения. Разработка инновационных методов лечения рака и улучшение результатов лечения пациентов могут быть ускорены путем решения проблем, с которыми сталкиваются повторно используемые лекарства, и использования их уникальных возможностей.
Это поднимает вопрос о том, стоит ли больше концентрироваться на клинической разработке одобренных препаратов, которые могут использоваться для лечения рака, поскольку их эффективность доказана в доклинических и ранних клинических исследованиях, а не на открытии новых молекул, что требует больших затрат и времени.
ССЫЛКИ
- Piña-Sánchez, P.; Chávez-González, A.; Ruiz-Tachiquín, M.; Vadillo, E.; Monroy-García, A.; Montesinos, J.J.; Grajales, R.; de la Barrera, M.G.; Mayani, H. Cancer biology, epidemiology, and treatment in the 21st century: Current status and future challenges from a biomedical perspective. Cancer Control. 2021, 28, 10732748211038735. [Google Scholar] [CrossRef] [PubMed]
- National Institutes of Health. NIH Curriculum Supplement Series; The Institutes: Malvern, PA, USA, 2007. Available online: https://www.ncbi.nlm.nih.gov/books/NBK20362/ (accessed on 16 November 2024).
- Cooper, G.M.; Hausman, R.E. The development and causes of cancer. Cell A Mol. Approach 2000, 2, 725–766. [Google Scholar]
- Correia, A.S.; Gärtner, F.; Vale, N. Drug combination and repurposing for cancer therapy: The example of breast cancer. Heliyon 2021, 7, e05948. [Google Scholar] [CrossRef] [PubMed]
- Brown, J.S.; Amend, S.R.; Austin, R.H.; Gatenby, R.A.; Hammarlund, E.U.; Pienta, K.J. Updating the definition of cancer. Cancer Res. 2023, 21, 1142–1147. [Google Scholar] [CrossRef] [PubMed]
- Goodman, E.N. What is the Environment Doing to Our Genes? A Pedigree Analysis of the Possible Genetic Basis of a Set of Familial Clinical Disorders; Encompass: Tonbridge, UK, 2022. [Google Scholar]
- Ramalingam, S. (Ed.) Cancer Genes; Bentham Science Publishers: Sharjah, United Arab Emirates, 2023. [Google Scholar]
- Khan, M.; Pelengaris, S. (Eds.) The Molecular Biology of Cancer: A Bridge from Bench to Bedside; John Wiley & Sons: Hoboken, NJ, USA, 2013; Available online: https://library.iau.edu.sa/scholarly-journals/molecular-biology-cancer-bridge-bench-bedside-2nd/docview/1349242751/se-2 (accessed on 16 November 2024).
- Hejmadi, M. Introduction to Cancer Biology; Bookboon: London, UK, 2014. [Google Scholar]
- Greenwald, P.; Dunn, B.K. Landmarks in the history of cancer epidemiology. Cancer Res. 2009, 69, 2151–2162. [Google Scholar] [CrossRef]
- Almatroudi, A. The incidence rate of colorectal cancer in Saudi Arabia: An observational descriptive epidemiological analysis. J. Gen. Med. 2020, 977–990. [Google Scholar] [CrossRef]
- Alqahtani, W.S.; Almufareh, N.A.; Domiaty, D.M.; Albasher, G.; Alduwish, M.A.; Alkhalaf, H.; Almuzzaini, B.; Al-Marshidy, S.S.; Alfraihi, R.; Elasbali, A.M.; et al. Epidemiology of cancer in Saudi Arabia thru 2010–2019: A systematic review with constrained meta-analysis. AIMS Public Health 2020, 7, 679. [Google Scholar] [CrossRef]
- Basudan, A.M. Breast cancer incidence patterns in the Saudi female population: A 17-year retrospective analysis. Medicina 2022, 58, 1617. [Google Scholar] [CrossRef]
- Elwali, N.E.; Jarrah, O.; Alzahrani, S.G.; Alharbi, M.B.; Alhejaily, A.G.; Alsharm, A.; Elhassan, M. Colorectal cancer in Saudi Arabia: The way forward. Asian Pac. J. Cancer Prev. APJCP 2023, 24, 13. [Google Scholar] [CrossRef]
- Elwali, N.E.; Jarrah, O.; Alzahrani, S.G.; Alharbi, M.B.; Alhejaily, A.G.; Alsharm, A.; Elhassan, M. Patterns of thyroid cancer mortality and incidence in Saudi Arabia: A 30-year study. Diagnostics 2022, 12, 2716. [Google Scholar] [CrossRef]
- Youk, T.M.; Hong, J.H.; Park, B.K.; Park, Y.M.; Park, E.-C. Estimation of the Three Phases by Direct Cost of Care for Non-Surviving Patients with Cancer: A National Population-Based Patient-Level Study. Cancer 2024, 15, 20. [Google Scholar] [CrossRef] [PubMed]
- Sleire, L.; Førde, H.E.; Netland, I.A.; Leiss, L.; Skeie, B.S.; Enger, P.O. Drug repurposing in cancer. Res. 2017, 124, 74–91. [Google Scholar] [CrossRef] [PubMed]
- Kulkarni, V.S.; Alagarsamy, V.; Solomon, V.R.; Jose, P.A.; Murugesan, S. Drug repurposing: An effective tool in modern drug discovery. J. Bioorganic Chem. 2023, 49, 157–166. [Google Scholar] [CrossRef] [PubMed]
- Song, J.W.; Chung, K.C.M. Observational studies: Cohort and case-control studies. Reconstr. Surg. 2010, 126, 2234–2242. [Google Scholar] [CrossRef]
- Weth, F.R.; Hoggarth, G.B.; Weth, A.F.; Paterson, E.; White, M.P.J.; Tan, S.T.; Peng, L.; Gray, C. Unlocking hidden potential: Advancements, approaches, and obstacles in repurposing drugs for cancer therapy. J. Cancer 2024, 130, 703–715. [Google Scholar] [CrossRef]
- Cheng, X.; Zhao, W.; Zhu, M.; Wang, B.; Wang, X.; Yang, X.; Huang, Y.; Tan, M.; Li, J. Drug repurposing for cancer treatment through global propagation with a greedy algorithm in a multilayer network. Cancer Biol. Med. 2022, 19, 74. [Google Scholar] [CrossRef] [PubMed]
- Sung, H.; Ferlay, J.; Siegel, R.L.; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA A Cancer J. Clin. 2021, 71, 209–249. [Google Scholar] [CrossRef]
- Li, M.; Zhang, Z.; Li, L.; Wang, X. An algorithm to quantify intratumor heterogeneity based on alterations of gene expression profiles. Biol. 2020, 3, 505. [Google Scholar] [CrossRef]
- Turnbull, A.K.; Selli, C.; Martinez-Perez, C.; Fernando, A.; Renshaw, L.; Keys, J.; Figueroa, J.D.; He, X.; Tanioka, M.; Munro, A.F.; et al. Unlocking the transcriptomic potential of formalin-fixed paraffin embedded clinical tissues: Comparison of gene expression profiling approaches. BMC Bioinform. 2020, 21, 1–10. [Google Scholar] [CrossRef]
- Rheinbay, E.; Nielsen, M.M.; Abascal, F.; Wala, J.A.; Shapira, O.; Tiao, G.; Hornshøj, H.; Hess, J.M.; Juul, R.I.; Lin, Z.; et al. Analyses of non-coding somatic drivers in 2,658 cancer whole genomes. Nature 2020, 578, 102–111. [Google Scholar] [CrossRef]
- Hanahan, D.; Weinberg, R.A. Hallmarks of cancer: The next generation. Cell 2011, 144, 646–674. [Google Scholar] [CrossRef] [PubMed]
- World Health Organization. WHO Report on Cancer: Setting Priorities, Investing Wisely and Providing Care for All. World Health Organization, 2020. Licence: CC BY-NC-SA 3.0 IGO. Available online: https://apps.who.int/iris/handle/10665/330745 (accessed on 16 November 2024).
- Creighton, C.J. Making use of cancer genomic databases. Curr. Protoc. Mol. Biol. 2018, 121, 14–19. [Google Scholar] [CrossRef] [PubMed]
- Pushpakom, S.; Iorio, F.; Eyers, P.A.; Escott, K.J.; Hopper, S.; Wells, A.; Doig, A.; Guilliams, T.; Latimer, J.; McNamee, C.; et al. Drug repurposing: Progress, challenges and recommendations. Nature reviews. Drug Discov. 2019, 18, 41–58. [Google Scholar] [CrossRef] [PubMed]
- Schcolnik-Cabrera, A.; Juárez-López, D.; Duenas-Gonzalez, A. Perspectives on Drug Repurposing. Med. Chem. 2021, 28, 2085–2099. [Google Scholar] [CrossRef] [PubMed]
- Schein, C.H. Repurposing approved drugs for cancer therapy. Br. Med. Bull. 2021, 137, 13–27. [Google Scholar] [CrossRef]
- Rodrigues, R.; Duarte, D.; Vale, N. Drug repurposing in cancer therapy: Influence of patient’s genetic background in breast cancer treatment. J. Mol. Sci. 2022, 23, 4280. [Google Scholar] [CrossRef]
- Aggarwal, S.; Verma, S.S.; Aggarwal, S.; Gupta, S.C. Drug repurposing for breast cancer therapy: Old weapon for new battle. Cancer Biol. 2021, 68, 8–20. [Google Scholar] [CrossRef]
- Elwood, P.; Morgan, G.; Watkins, J.; Protty, M.; Mason, M.; Adams, R.; Dolwani, S.; Pickering, J.; Delon, C.; Longley, M. Aspirin and cancer treatment: Systematic reviews and meta-analyses of evidence: For and against. J. Cancer 2024, 130, 3–8. [Google Scholar] [CrossRef]
- Zhang, X.; Du, R.; Luo, N.; Xiang, R.; Shen, W. Aspirin mediates histone methylation that inhibits inflammation-related stemness gene expression to diminish cancer stemness via COX-independent manner. Stem Cell Res. Ther. 2020, 11, 1–15. [Google Scholar] [CrossRef]
- Guo, Y.; Liu, Y.; Zhang, C.; Su, Z.-Y.; Li, W.; Huang, M.-T.; Kong, A.-N.T. The epigenetic effects of aspirin: The modification of histone H3 lysine 27 acetylation in the prevention of colon carcinogenesis in azoxymethane-and dextran sulfate sodium-treated CF-1 mice. Carcinogenesis 2016, 37, 616–624. [Google Scholar] [CrossRef]
- Elwood, P.; Protty, M.; Morgan, G.; Pickering, J.; Delon, C.; Watkins, J. Aspirin and cancer: Biological mechanisms and clinical outcomes. Open Biol. 2022, 12, 220124. [Google Scholar] [CrossRef] [PubMed]
- Motta, R.; Cabezas-Camarero, S.; Torres-Mattos, C.; Riquelme, A.; Calle, A.; Figueroa, A.; Sotelo, M.J. Immunotherapy in microsatellite instability metastatic colorectal cancer: Current status and future perspectives. Clin. Transl. Res. 2021, 7, 511. [Google Scholar] [PubMed] [PubMed Central]
- Nounu, A.; Greenhough, A.; Heesom, K.J.; Richmond, R.C.; Zheng, J.; Weinstein, S.J.; Albanes, D.; Baron, J.A.; Hopper, J.L.; Figueiredo, J.C.; et al. A combined proteomics and Mendelian randomization approach to investigate the effects of aspirin-targeted proteins on colorectal cancer. Cancer Epidemiol. Biomark. Prev. 2021, 30, 564–575. [Google Scholar] [CrossRef] [PubMed]
- Malik, J.A.; Ahmed, S.; Jan, B.; Bender, O.; Al Hagbani, T.; Alqarni, A.; Anwar, S. Drugs repurposed: An advanced step towards the treatment of breast cancer and associated challenges. Pharmacother. 2022, 145, 112375. [Google Scholar] [CrossRef]
- Lord, S.R.; Harris, A.L. Is it still worth pursuing the repurposing of metformin as a cancer therapeutic? J. Cancer 2023, 128, 958–966. [Google Scholar] [CrossRef]
- Jourdan, J.-P.; Bureau, R.; Rochais, C.; Dallemagne, P. Drug repositioning: A brief overview. Pharm. Pharmacol. 2020, 72, 1145–1151. [Google Scholar] [CrossRef]
- Siddiqui, S.; Deshmukh, A.J.; Mudaliar, P.; Nalawade, A.J.; Iyer, D.; Aich, J. Drug repurposing: Re-inventing therapies for cancer without re-entering the development pipeline—A review. Egypt. Natl. Cancer Inst. 2022, 34, 33. [Google Scholar] [CrossRef]
- Zhu, L.; Yang, K.; Ren, Z.; Yin, D.; Zhou, Y. Metformin as anticancer agent and adjuvant in cancer combination therapy: Current progress and future prospect. Oncol. Vol. 2024, 44, 101945. [Google Scholar] [CrossRef]
- LaMoia, T.E.; Shulman, G.I. Cellular and molecular mechanisms of metformin action. Rev. 2021, 42, 77–96. [Google Scholar] [CrossRef]
- Bose, S.; Zhang, C.; Le, A. Glucose metabolism in cancer: The Warburg effect and beyond. Adv. Exp. Med. Biol. 2021, 1311, 3–15. Available online: http://www.springer.com/series/5584 (accessed on 16 November 2024).
- Bailey, C.J. Metformin: Historical overview. Diabetologia 2017, 60, 1566–1576. [Google Scholar] [CrossRef] [PubMed]
- Hunter, R.W.; Hughey, C.C.; Lantier, L.; Sundelin, E.I.; Peggie, M.; Zeqiraj, E.; Sicheri, F.; Jessen, N.; Wasserman, D.H.; Sakamoto, K. Metformin reduces liver glucose production by inhibition of fructose-1-6-bisphosphatase. Med. 2018, 24, 1395–1406. [Google Scholar] [CrossRef] [PubMed]
- Qi, J.; He, P.; Yao, H.; Song, R.; Ma, C.; Cao, M.; Cui, B.; Ning, G. Cancer risk among patients with type 2 diabetes: A real-world study in Shanghai, China. Diabetes 2019, 11, 878–883. [Google Scholar] [CrossRef] [PubMed]
- Olatunde, A.; Nigam, M.; Singh, R.K.; Panwar, A.S.; Lasisi, A.; Alhumaydhi, F.A.; Kumar, V.J.; Mishra, A.P.; Sharifi-Rad, J. Cancer and diabetes: The interlinking metabolic pathways and repurposing actions of antidiabetic drugs. Cancer Cell Int. 2021, 21, 1–27. [Google Scholar] [CrossRef]
- Liu, Y.-C.; Nguyen, P.-A.; Humayun, A.; Chien, S.-C.; Yang, H.-C.; Asdary, R.N.; Syed-Abdul, S.; Hsu, M.-H.; Moldovan, M.; Yen, Y.; et al. Does long-term use of antidiabetic drugs changes cancer risk? Medicine 2019, 98, e17461. [Google Scholar] [CrossRef]
- Hijazi, M.A.; Gessner, A.; El-Najjar, N. Repurposing of chronically used drugs in cancer therapy: A chance to grasp. Cancers 2023, 15, 3199. [Google Scholar] [CrossRef]
- Kirtonia, A.; Gala, K.; Fernandes, S.G.; Pandya, G.; Pandey, A.K.; Sethi, G.; Khattar, E.; Garg, M. Repurposing of drugs: An attractive pharmacological strategy for cancer therapeutics. Cancer Biol. 2021, 68, 258–278. [Google Scholar] [CrossRef]
- Dąbrowski, M. Diabetes, antidiabetic medications and cancer risk in type 2 diabetes: Focus on SGLT-2 inhibitors. J. Mol. Sci. 2021, 22, 1680. [Google Scholar] [CrossRef]
- Kole, L.; Sarkar, M.; Deb, A.; Giri, B. Pioglitazone, an anti-diabetic drug requires sustained MAPK activation for its anti-tumor activity in MCF7 breast cancer cells, independent of PPAR-γ Pharmacol. Rep. 2016, 68, 144–154. [Google Scholar] [CrossRef]
- Chi, T.; Wang, M.; Wang, X.; Yang, K.; Xie, F.; Liao, Z.; Wei, P. PPAR-γ modulators as current and potential cancer treatments. Oncol. 2021, 11, 737776. [Google Scholar] [CrossRef]
- Tan, Y.; Wang, M.; Yang, K.; Chi, T.; Liao, Z.; Wei, P. PPAR-α modulators as current and potential cancer treatments. Oncol. 2021, 11, 599995. [Google Scholar] [CrossRef] [PubMed]
- Mirza, A.Z.; Althagafi, I.I.; Shamshad, H. Role of PPAR receptor in different diseases and their ligands: Physiological importance and clinical implications. J. Med. Chem. 2019, 166, 502–513. [Google Scholar] [CrossRef] [PubMed]
- Galal, M.A.; Al-Rimawi, M.; Hajeer, A.; Dahman, H.; Alouch, S.; Aljada, A. Metformin: A Dual-Role Player in Cancer Treatment and Prevention. J. Mol. Sci. 2024, 25, 4083. [Google Scholar] [CrossRef] [PubMed]
- Hua, Y.; Zheng, Y.; Yao, Y.; Jia, R.; Ge, S.; Zhuang, A. Metformin and cancer hallmarks: Shedding new lights on therapeutic repurposing. Transl. Med. 2023, 21, 403. [Google Scholar] [CrossRef]
- Brown, J.R.; Chan, D.K.; Shank, J.J.; Griffith, K.A.; Fan, H.; Szulawski, R.; Yang, K.; Reynolds, R.K.; Johnston, C.; McLean, K.; et al. Phase II clinical trial of metformin as a cancer stem cell–targeting agent in ovarian cancer. JCI Insight 2020, 5, e133247. [Google Scholar] [CrossRef]
- Pantziarka, P.; Bouche, G.; Meheus, L.; Sukhatme, V.; Sukhatme, V.P. Repurposing Drugs in Oncology (ReDO)—Mebendazole as an anticancer agent. Ecancermedicalscience 2014, 8, 443. [Google Scholar] [CrossRef]
- Laudisi, F.; Marônek, M.; Di Grazia, A.; Monteleone, G.; Stolfi, C. Repositioning of anthelmintic drugs for the treatment of cancers of the digestive system. J. Mol. Sci. 2020, 21, 4957. [Google Scholar] [CrossRef]
- Younis, N.S.; Ghanim, A.M.H.; Saber, S. Mebendazole augments sensitivity to sorafenib by targeting MAPK and BCL-2 signalling in n-nitrosodiethylamine-induced murine hepatocellular carcinoma. Rep. 2019, 9, 19095. [Google Scholar] [CrossRef]
- Chen, H.; Weng, Z.; Xu, C. Albendazole suppresses cell proliferation and migration and induces apoptosis in human pancreatic cancer cells. Drugs 2020, 31, 431–439. [Google Scholar] [CrossRef]
- Lee, M.; Chen, Y.; Hsu, Y.; Lin, B. Niclosamide inhibits the cell proliferation and enhances the responsiveness of esophageal cancer cells to chemotherapeutic agents. Rep. 2020, 43, 549–561. [Google Scholar] [CrossRef]
- Xing, X.; Zhou, Z.; Peng, H.; Cheng, S. Anticancer role of flubendazole: Effects and molecular mechanisms. Lett. 2024, 28, 558. [Google Scholar] [CrossRef]
- Venugopal, S.; Kaur, B.; Verma, A.; Wadhwa, P.; Magan, M.; Hudda, S.; Kakoty, V. Recent advances of benzimidazole as anticancer agents. Biol. Drug Des. 2023, 102, 357–376. [Google Scholar] [CrossRef]
- Mohi-Ud-Din, R.; Chawla, A.; Sharma, P.; Mir, P.A.; Potoo, F.H.; Reiner, Ž.; Reiner, I.; Ateşşahin, D.A.; Sharifi-Rad, J.; Mir, R.H.; et al. Repurposing approved non-oncology drugs for cancer therapy: A comprehensive review of mechanisms, efficacy, and clinical prospects. J. Med. Res. 2023, 28, 345. [Google Scholar] [CrossRef]
- Guerini, A.E.; Triggiani, L.; Maddalo, M.; Bonù, M.L.; Frassine, F.; Baiguini, A.; Alghisi, A.; Tomasini, D.; Borghetti, P.; Pasinetti, N.; et al. Mebendazole as a candidate for drug repurposing in oncology: An extensive review of current literature. Cancers 2019, 11, 1284. [Google Scholar] [CrossRef]
- Rushworth, L.K.; Hewit, K.; Munnings-Tomes, S.; Somani, S.; James, D.; Shanks, E.; Dufès, C.; Straube, A.; Patel, R.; Leung, H.Y. Repurposing screen identifies mebendazole as a clinical candidate to synergise with docetaxel for prostate cancer treatment. J. Cancer 2020, 122, 517–527. [Google Scholar] [CrossRef]
- Zhang, Z.; Ji, J.; Liu, H. Drug repurposing in oncology: Current evidence and future direction. Med. Chem. 2021, 28, 2175–2194. [Google Scholar] [CrossRef]
- Zhang, Z.; Zhou, L.; Xie, N.; Nice, E.C.; Zhang, T.; Cui, Y.; Huang, C. Overcoming cancer therapeutic bottleneck by drug repurposing. Signal Transduct. Target. Ther. 2020, 5, 113. [Google Scholar] [CrossRef]
- Lu, L.; Dong, J.; Wang, L.; Xia, Q.; Zhang, D.; Kim, H.; Yin, T.; Fan, S.; Shen, Q. Activation of STAT3 and Bcl-2 and reduction of reactive oxygen species (ROS) promote radioresistance in breast cancer and overcome of radioresistance with niclosamide. Oncogene 2018, 37, 5292–5304. [Google Scholar] [CrossRef]
- Cao, B.; Li, J.; Zhu, J.; Shen, M.; Han, K.; Zhang, Z.; Yu, Y.; Wang, Y.; Wu, D.; Chen, S.; et al. The antiparasitic clioquinol induces apoptosis in leukemia and myeloma cells by inhibiting histone deacetylase activity. Biol. Chem. 2013, 288, 34181–34189. [Google Scholar] [CrossRef]
- Cao, B.; Shen, M.; Wu, D.; Du, J.; Zhu, J.; Chen, S.; Sun, A.; Tang, X.; Xu, Z.; Kong, Y.; et al. The Proteasomal Inhibitor Clioquinol Induces Apoptosis in Leukemia and Myeloma Cells by Inhibiting Histone Deacetylase Activity. Blood 2012, 120, 2449. [Google Scholar] [CrossRef]
- Borcherding, N.; Jethava, Y.; Vikas, P. Repurposing anticancer drugs for COVID-19 treatment. Drug design, development and therapy. Drug Des. Dev. Ther. 2020, 5045–5058. [Google Scholar] [CrossRef]
- Pfab, C.; Schnobrich, L.; Eldnasoury, S.; Gessner, A.; El-Najjar, N. Repurposing of antimicrobial agents for cancer therapy: What do we know? Cancers 2021, 13, 3193. [Google Scholar] [CrossRef]
- Aldea, M.; Michot, J.-M.; Danlos, F.-X.; Ribas, A.; Soria, J.-C. Repurposing of anticancer drugs expands possibilities for antiviral and anti-inflammatory discovery in COVID-19. Cancer Discov. 2021, 11, 1336–1344. [Google Scholar] [CrossRef]
- Pal, D.; Song, I.-H.; Warkad, S.D.; Song, K.-S.; Yeom, G.S.; Saha, S.; Shinde, P.B.; Nimse, S.B. Indazole-based microtubule-targeting agents as potential candidates for anticancer drugs discovery. Bioorganic Chem. 2022, 122, 105735. [Google Scholar] [CrossRef]
- De Lellis, L.; Veschi, S.; Tinari, N.; Mokini, Z.; Carradori, S.; Brocco, D.; Florio, R.; Grassadonia, A.; Cama, A. Drug repurposing, an attractive strategy in pancreatic cancer treatment: Preclinical and clinical updates. Cancers 2021, 13, 3946. [Google Scholar] [CrossRef]
- Regulska, K.; Regulski, M.; Karolak, B.; Murias, M.; Stanisz, B. Can cardiovascular drugs support cancer treatment? The rationale for drug repurposing. Drug Discov. Today 2019, 24, 1059–1065. [Google Scholar] [CrossRef]
- Hashemzehi, M.; Rahmani, F.; Khoshakhlagh, M.; Avan, A.; Asgharzadeh, F.; Barneh, F.; Moradi-Marjaneh, R.; Soleimani, A.; Fiuji, H.; Ferns, G.A.; et al. Angiotensin receptor blocker Losartan inhibits tumor growth of colorectal cancer. Excli J. 2021, 20, 506. [Google Scholar] [CrossRef]
- Tan, X.; Guo, S.; Wang, C. Propranolol in the treatment of infantile hemangiomas. Clinical, Cosmetic and Investigational Dermatology Clin. Cosmet. Investig. Dermatol. 2021, 1155–1163. [CrossRef]
- Kwak, J.H.; Yang, A.; Jung, H.L.; Kim, H.J.; Kim, D.S.; Shim, J.Y.; Shim, J.W. Cardiac Evaluation before and after Oral Propranolol Treatment for Infantile Hemangiomas. Clin. Med. 2024, 13, 3332. [Google Scholar] [CrossRef]
- Benish, M.; Bartal, I.; Goldfarb, Y.; Levi, B.; Avraham, R.; Raz, A.; Ben-Eliyahu, S. Perioperative use of β-blockers and COX-2 inhibitors may improve immune competence and reduce the risk of tumor metastasis. Surg. Oncol. 2008, 15, 2042–2052. [Google Scholar] [CrossRef]
- Li, Z.; Li, Q.; Wu, J.; Wang, M.; Yu, J. Artemisinin and its derivatives as a repurposing anticancer agent: What else do we need to do? Molecules 2016, 21, 1331. [Google Scholar] [CrossRef]
- Chae, Y.K.; Valsecchi, M.E.; Kim, J.; Bianchi, A.L.; Khemasuwan, D.; Desai, A.; Tester, W. Reduced risk of breast cancer recurrence in patients using ACE inhibitors, ARBs, and/or statins. Cancer Investig. 2011, 29, 585–593. [Google Scholar] [CrossRef]
- Coulson, R.; Liew, S.H.; Connelly, A.A.; Yee, N.S.; Deb, S.; Kumar, B.; Vargas, A.C.; O’toole, S.A.; Parslow, A.C.; Poh, A.; et al. The angiotensin receptor blocker, Losartan, inhibits mammary tumor development and progression to invasive carcinoma. Oncotarget 2017, 8, 18640–18656. [Google Scholar] [CrossRef]
- Vinson, G.P. Why isn’t the angiotensin type 1 receptor a target in cancer? Oncotarget 2017, 8, 18618. [Google Scholar] [CrossRef]
- Tabatabai, E.; Khazaei, M.; Asgharzadeh, F.; Nazari, S.E.; Shakour, N.; Fiuji, H.; Ziaeemehr, A.; Mostafapour, A.; Parizadeh, M.R.; Nouri, M.; et al. Inhibition of angiotensin II type 1 receptor by candesartan reduces tumor growth and ameliorates fibrosis in colorectal cancer. Excli J. 2021, 20, 863. [Google Scholar] [CrossRef]
- Asgharzadeh, F.; Mostafapour, A.; Ebrahimi, S.; Amerizadeh, F.; Sabbaghzadeh, R.; Hassanian, S.M.; Fakhraei, M.; Farshbaf, A.; Ferns, G.A.; Giovannetti, E.; et al. Inhibition of angiotensin pathway via valsartan reduces tumor growth in models of colorectal cancer. Toxicol. Appl. 2022, 440, 115951. [Google Scholar] [CrossRef]
- Pantziarka, P.; Verbaanderd, C.; Capistrano, R.; Crispino, S.; Gyawali, B.; Rooman, I.; Van Nuffel, A.M.; Meheus, L.; Sukhatme, V.P.; Bouche, G. ReDO_DB: The repurposing drugs in oncology database. Ecancermedicalscience 2018, 12, 886. [Google Scholar] [CrossRef]
- Le Provost, K.C.; Kepp, O.; Kroemer, G.; Bezu, L. Trial watch: Beta-blockers in cancer therapy. OncoImmunology 2023, 12, 2284486. [Google Scholar] [CrossRef]
- Bravo-Calderón, D.M.; Assao, A.; Garcia, N.G.; Coutinho-Camillo, C.M.; Roffé, M.; Germano, J.N.; Oliveira, D.T. Beta adrenergic receptor activation inhibits oral cancer migration and invasiveness. Oral Biol. 2020, 118, 104865. [Google Scholar] [CrossRef]
- Kwon, S.Y.; Chun, K.J.; Kil, H.K.; Jung, N.; Shin, H.-A.; Jang, J.Y.; Choi, H.G.; Oh, K.-H.; Kim, M.-S. β2 adrenergic receptor expression and the effects of norepinephrine and propranolol on various head and neck cancer subtypes. Lett. 2021, 22, 1–8. [Google Scholar] [CrossRef]
- Shebl, R. Anticancer potential of captopril and botulinum toxin type-A and associated p53 gene apototic stimulating activity. J. Pharm. Res. IJPR 2019, 18, 1967. [Google Scholar] [CrossRef]
- Hassani, B.; Attar, Z.; Firouzabadi, N. The renin-angiotensin-aldosterone system (RAAS) signaling pathways and cancer: Foes versus allies. Cancer Cell Int. 2023, 23, 254. [Google Scholar] [CrossRef]
- Fukushiro-Lopes, D.; Hegel, A.D.; Russo, A.; Senyuk, V.; Liotta, M.; Beeson, G.C.; Beeson, C.C.; Burdette, J.; Potkul, R.K.; Gentile, S. Repurposing Kir6/SUR2 channel activator minoxidil to arrests growth of gynecologic cancers. Pharmacol. 2020, 11, 577. [Google Scholar] [CrossRef]
- Salanci, Š.; Vilková, M.; Martinez, L.; Mirossay, L.; Michalková, R.; Mojžiš, J. The Induction of G2/M Phase Cell Cycle Arrest and Apoptosis by the Chalcone Derivative 1C in Sensitive and Resistant Ovarian Cancer Cells Is Associated with ROS Generation. J. Mol. Sci. 2024, 25, 7541. [Google Scholar] [CrossRef]
- Qiu, S.; Fraser, S.P.; Pires, W.; Djamgoz, M.B.A. Anti-invasive effects of minoxidil on human breast cancer cells: Combination with ranolazine. Exp. Metastasis 2022, 39, 679–689. [Google Scholar] [CrossRef]
- Carlos-Escalante, J.A.; de Jesús-Sánchez, M.; Rivas-Castro, A.; Pichardo-Rojas, P.S.; Arce, C.; Wegman-Ostrosky, T. The use of antihypertensive drugs as coadjuvant therapy in cancer. Oncol. 2021, 11, 660943. [Google Scholar] [CrossRef]
- Ioakeim-Skoufa, I.; Tobajas-Ramos, N.; Menditto, E.; Aza-Pascual-Salcedo, M.; Gimeno-Miguel, A.; Orlando, V.; González-Rubio, F.; Fanlo-Villacampa, A.; Lasala-Aza, C.; Ostasz, E.; et al. Drug repurposing in oncology: A systematic review of randomized controlled clinical trials. Cancers 2023, 15, 2972. [Google Scholar] [CrossRef]
- Ribeiro, E.; Vale, N. Repurposing of the Drug Tezosentan for Cancer Therapy. Issues Mol. Biol. 2023, 45, 5118–5131. [Google Scholar] [CrossRef]
- Wang, R.; Dashwood, R.H. Endothelins and their receptors in cancer: Identification of therapeutic targets. Res. 2011, 63, 519–524. [Google Scholar] [CrossRef]
- Lian, X.; Wang, G.; Zhou, H.; Zheng, Z.; Fu, Y.; Cai, L. Anticancer properties of fenofibrate: A repurposing use. Cancer 2018, 9, 1527. [Google Scholar] [CrossRef]
- Chen, L.; Peng, J.; Wang, Y.; Jiang, H.; Wang, W.; Dai, J.; Tang, M.; Wei, Y.; Kuang, H.; Xu, G.; et al. Fenofibrate-induced mitochondrial dysfunction and metabolic reprogramming reversal: The anti-tumor effects in gastric carcinoma cells mediated by the PPAR pathway. Am. J. Transl. 2020, 12, 428. [Google Scholar] [PubMed] [PubMed Central]
- Kale, V.P.; Amin, S.G.; Pandey, M.K. Targeting ion channels for cancer therapy by repurposing the approved drugs. Et Biophys. Acta (BBA)-Biomembr. 2015, 1848, 2747–2755. [Google Scholar] [CrossRef]
- Zhao, J.; Li, M.; Xu, J.; Cheng, W. The modulation of ion channels in cancer chemo-resistance. Oncol. 2022, 12, 945896. [Google Scholar] [CrossRef]
- Altamura, C.; Gavazzo, P.; Pusch, M.; Desaphy, J.-F. Ion channel involvement in tumor drug resistance. Pers. Med. 2022, 12, 210. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- Leanza, L.; Managò, A.; Zoratti, M.; Gulbins, E.; Szabo, I. Pharmacological targeting of ion channels for cancer therapy: In vivo evidences. Biochim. Et Biophys. Acta (BBA)-Mol. Cell Res. 2016, 1863, 1385–1397. [Google Scholar] [CrossRef]
- Bell, D.C.; Leanza, L.; Gentile, S.; Sauter, D.R. News and views on ion channels in cancer: Is cancer a channelopathy? Pharmacol. 2023, 14, 1258933. [Google Scholar] [CrossRef]
- Li, M.; Tian, P.; Zhao, Q.; Ma, X.; Zhang, Y. Potassium channels: Novel targets for tumor diagnosis and chemoresistance. Oncol. 2023, 12, 1074469. [Google Scholar] [CrossRef]
- Dupuy, M.; Gueguinou, M.; Potier-Cartereau, M.; Lézot, F.; Papin, M.; Chantôme, A.; Rédini, F.; Vandier, C.; Verrecchia, F. SKCa-and Kv1-type potassium channels and cancer: Promising therapeutic targets? Pharmacol. 2023, 216, 115774. [Google Scholar] [CrossRef]
- Luis, E.; Anaya-Hernández, A.; León-Sánchez, P.; Durán-Pastén, M.L. The Kv10. 1 channel: A promising target in cancer. J. Mol. Sci. 2022, 23, 8458. [Google Scholar] [CrossRef]
- Sakellakis, M.; Yoon, S.M.; Reet, J.; Chalkias, A. Novel insights into voltage-gated ion channels: Translational breakthroughs in medical oncology. Channels 2024, 18, 2297605. [Google Scholar] [CrossRef]
- Pasello, G.; Urso, L.; Conte, P.; Favaretto, A. Effects of sulfonylureas on tumor growth: A review of the literature. 2013, 18, 1118–1125. [Google Scholar] [CrossRef]
- Zúñiga, L.; Cayo, A.; González, W.; Vilos, C.; Zúñiga, R. Potassium channels as a target for cancer therapy: Current perspectives. OncoTargets Ther. 2022, 15, 783. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- Wong, B.-S.; Chiu, L.-Y.; Tu, D.-G.; Sheu, G.-T.; Chan, T.-T. Anticancer effects of antihypertensive L-type calcium channel blockers on chemoresistant lung cancer cells via autophagy and apoptosis. Cancer Manag. Res. 2020, 1913–1927. [Google Scholar] [CrossRef]
- Huang, T.; Zhou, J.; Wang, J. Calcium and calcium-related proteins in endometrial cancer: Opportunities for pharmacological intervention. Int. J. Biol. Sci. 2022, 18, 1065. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- Wang, X.; Zhao, J.; Marostica, E.; Yuan, W.; Jin, J.; Zhang, J.; Li, R.; Tang, H.; Wang, K.; Li, Y.; et al. A pathology foundation model for cancer diagnosis and prognosis prediction. Nature 2024, 634, 970–978. [Google Scholar] [CrossRef]
- Parvathaneni, V.; Elbatanony, R.S.; Goyal, M.; Chavan, T.; Vega, N.; Kolluru, S.; Muth, A.; Gupta, V.; Kunda, N.K. Repurposing bedaquiline for effective non-small cell lung cancer (NSCLC) therapy as inhalable cyclodextrin-based molecular inclusion complexes. J. Mol. Sci. 2021, 22, 4783. [Google Scholar] [CrossRef]
- Fiorillo, M.; Lamb, R.; Tanowitz, H.B.; Cappello, A.R.; Martinez-Outschoorn, U.E.; Sotgia, F.; Lisanti, M.P. Bedaquiline, an FDA-approved antibiotic, inhibits mitochondrial function and potently blocks the proliferative expansion of stem-like cancer cells (CSCs). Aging 2016, 8, 1593. [Google Scholar] [CrossRef] [PubMed]
- Fu, L.; Jin, W.; Zhang, J.; Zhu, L.; Lu, J.; Zhen, Y.; Zhang, L.; Ouyang, L.; Liu, B.; Yu, H. Repurposing non-oncology small-molecule drugs to improve cancer therapy: Current situation and future directions. Acta Pharm. Sin. B 2022, 12, 532–557. [Google Scholar] [CrossRef]
- Li, J.; Qin, Y.; Zhao, C.; Zhang, Z.; Zhou, Z. Tetracycline antibiotics: Potential anticancer drugs. J. Pharmacol. 2023, 956, 175949. [Google Scholar] [CrossRef]
- Dong, Z.; Abbas, M.N.; Kausar, S.; Yang, J.; Li, L.; Tan, L.; Cui, H. Biological functions and molecular mechanisms of antibiotic tigecycline in the treatment of cancers. J. Mol. Sci. 2019, 20, 3577. [Google Scholar] [CrossRef]
- Bailly, C.; Vergoten, G. A new horizon for the old antibacterial drug clofoctol. Drug Discov. Today 2021, 26, 1302–1310. [Google Scholar] [CrossRef]
- Wang, M.; Shim, J.S.; Li, R.; Dang, Y.; He, Q.; Das, M.; O Liu, J. Identification of an old antibiotic clofoctol as a novel activator of unfolded protein response pathways and an inhibitor of prostate cancer. J. Pharmacol. 2014, 171, 4478–4489. [Google Scholar] [CrossRef] [PubMed]
- van der Zanden, S.Y.; Qiao, X.; Neefjes, J. New insights into the activities and toxicities of the old anticancer drug doxorubicin. FEBS J. 2021, 288, 6095–6111. [Google Scholar] [CrossRef]
- Shandilya, M.; Sharma, S.; Das, P.P.; Charak, S. Molecular-level understanding of the anticancer action mechanism of anthracyclines. Precis. Med. Oncol. 2020. [Google Scholar] [CrossRef]
- Mukai, H.; Kogawa, T.; Matsubara, N.; Naito, Y.; Sasaki, M.; Hosono, A. A first-in-human Phase 1 study of epirubicin-conjugated polymer micelles (K-912/NC-6300) in patients with advanced or recurrent solid tumors. New Drugs 2017, 35, 307–314. [Google Scholar] [CrossRef]
- Pourgholami, M.H.; Mekkawy, A.H.; Badar, S.; Morris, D.L. Minocycline inhibits growth of epithelial ovarian cancer. Oncol. 2012, 125, 433–440. [Google Scholar] [CrossRef] [PubMed]
- Afshari, A.R.; Mollazadeh, H.; Sahebkar, A. Minocycline in treating glioblastoma multiforme: Far beyond a conventional antibiotic. Oncol. 2020, 2020, 8659802. [Google Scholar] [CrossRef]
- Reed, G.A.; Schiller, G.J.; Kambhampati, S.; Tallman, M.S.; Douer, D.; Minden, M.D.; Yee, K.W.; Gupta, V.; Brandwein, J.; Jitkova, Y.; et al. A Phase 1 study of intravenous infusions of tigecycline in patients with acute myeloid leukemia. Cancer Med. 2016, 5, 3031–3040. [Google Scholar] [CrossRef]
- Novella, P.; Salvatore, P.; Iula, D.V.; Catania, M.R.; Chiurazzi, F.; Raimondo, M.; Beneduce, G.; Cerchione, C.; Della Pepa, R.; Giordano, C.; et al. Tigecycline-Based Front-Line Antibiotic Therapy Significantly Decreases Mortality Among Patients with Neutropenic Enterocolitis Following Cytarabine-Containing Chemotherapy for the Remission Induction of Acute Myeloid Leukemia. Blood 2016, 128, 3550. [Google Scholar] [CrossRef]
- Nowakowska, J.; Radomska, D.; Czarnomysy, R.; Marciniec, K. Recent Development of Fluoroquinolone Derivatives as Anticancer Agents. Molecules 2024, 29, 3538. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- AbuBaih, R.H.; Fawzy, M.A.; Nazmy, M.H. The prospective potential of fluoroquinolones as anticancer agents. Mod. Res. 2023, 5, 4–10. [Google Scholar] [CrossRef]
- Zhou, W.; Wang, H.; Yang, Y.; Chen, Z.-S.; Zou, C.; Zhang, J. Chloroquine against malaria, cancers and viral diseases. Drug Discov. Today 2020, 25, 2012–2022. [Google Scholar] [CrossRef] [PubMed]
- Liu, Y.; Meng, Y.; Zhang, J.; Gu, L.; Shen, S.; Zhu, Y.; Wang, J. Pharmacology Progresses and Applications of Chloroquine in Cancer Therapy. J. Nanomed. 2024, 6777–6809. [Google Scholar] [CrossRef] [PubMed]
- Mauthe, M.; Orhon, I.; Rocchi, C.; Zhou, X.; Luhr, M.; Hijlkema, K.-J.; Coppes, R.P.; Engedal, N.; Mari, M.; Reggiori, F. Chloroquine inhibits autophagic flux by decreasing autophagosome-lysosome fusion. Autophagy 2018, 14, 1435–1455. [Google Scholar] [CrossRef] [PubMed]
- Vlachos, N.; Lampros, M.; Voulgaris, S.; Alexiou, G.A. Repurposing antipsychotics for cancer treatment. Biomedicines 2021, 9, 1785. [Google Scholar] [CrossRef] [PubMed]
- Lianos, G.D.; Alexiou, G.A.; Rausei, S.; Galani, V.; Mitsis, M.; Kyritsis, A.P. Repurposing antipsychotic drugs for cancer treatment: Current evidence and future perspectives. Expert Rev. Anticancer. Ther. 2022, 22, 131–134. [Google Scholar] [CrossRef]
- Moura, C.; Vale, N. The role of dopamine in repurposing drugs for oncology. Biomedicines 2023, 11, 1917. [Google Scholar] [CrossRef]
- Vasconcelos, M.H.; Palmeira, A.; Sousa, S.M.; Xavier, C.P.R. Repurposing some of the Well-Known Non-Steroid Anti-Inflammatory Drugs (NSAIDs) for Cancer Treatment. Top. Med. Chem. 2023, 23, 1171–1195. [Google Scholar] [CrossRef]
- Ozleyen, A.; Yilmaz, Y.B.; Donmez, S.; Atalay, H.N.; Antika, G.; Tumer, T.B. Looking at NSAIDs from a historical perspective and their current status in drug repurposing for cancer treatment and prevention. Cancer Res. Clin. Oncol. 2023, 149, 2095–2113. [Google Scholar] [CrossRef]
- Bin Joo, Y.; Jung, S.M.; Park, Y.-J.; Kim, K.-J.; Park, K.-S. Use of disease-modifying antirheumatic drugs after cancer diagnosis in rheumatoid arthritis patients. Rheum. Dis. 2022, 29, 162–170. [Google Scholar] [CrossRef]
- De Sousa-Coelho, A.L.; Fraqueza, G.; Aureliano, M. Repurposing Therapeutic Drugs Complexed to Vanadium in Cancer. Pharmaceuticals 2023, 17, 12. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- Calip, G.S.; Patel, P.R.; Sweiss, K.; Wu, Z.; Zhou, J.; Asfaw, A.A.; Adimadhyam, S.; Lee, T.A.; Chiu, B.C. Targets of biologic disease-modifying antirheumatic drugs and risk of multiple myeloma. J. Cancer 2020, 147, 1300–1305. [Google Scholar] [CrossRef] [PubMed]
- Aroosa, M.; Malik, J.A.; Ahmed, S.; Bender, O.; Ahemad, N.; Anwar, S. The evidence for repurposing anti-epileptic drugs to target cancer. Biol. Rep. 2023, 50, 7667–7680. [Google Scholar] [CrossRef] [PubMed]
- Sulsenti, R.; Frossi, B.; Bongiovanni, L.; Cancila, V.; Ostano, P.; Fischetti, I.; Enriquez, C.; Guana, F.; Chiorino, G.; Tripodo, C.; et al. Repurposing of the antiepileptic drug levetiracetam to restrain neuroendocrine prostate cancer and inhibit mast cell support to adenocarcinoma. Immunol. 2021, 12, 622001. [Google Scholar] [CrossRef] [PubMed]
- Malla, R.; Viswanathan, S.; Makena, S.; Kapoor, S.; Verma, D.; Raju, A.A.; Dunna, M.; Muniraj, N. Revitalizing Cancer Treatment: Exploring the Role of Drug Repurposing. Cancers 2024, 16, 1463. [Google Scholar] [CrossRef]
- Rizzo, A.; Donzelli, S.; Girgenti, V.; Sacconi, A.; Vasco, C.; Salmaggi, A.; Blandino, G.; Maschio, M.; Ciusani, E. In vitro antineoplastic effects of brivaracetam and lacosamide on human glioma cells. Exp. Clin. Cancer Res. 2017, 36, 1–13. [Google Scholar] [CrossRef]
- Moutal, A.; Villa, L.S.; Yeon, S.K.; Householder, K.T.; Park, K.D.; Sirianni, R.W.; Khanna, R. CRMP2 phosphorylation drives glioblastoma cell proliferation. Neurobiol. 2018, 55, 4403–4416. [Google Scholar] [CrossRef]
- Morales, X.; Peláez, R.; Garasa, S.; de Solórzano, C.O.; Rouzaut, A. CRMP2 as a candidate target to interfere with lung cancer cell migration. Biomolecules 2021, 11, 1533. [Google Scholar] [CrossRef]
- Costa, B.; Vale, N. Understanding Lamotrigine’s role in the CNS and possible future evolution. J. Mol. Sci. 2023, 24, 6050. [Google Scholar] [CrossRef]
- Kim, K.J.; Jeun, S.H.; Sung, K.-W. Lamotrigine, an antiepileptic drug, inhibits 5-HT3 receptor currents in NCB-20 neuroblastoma cells. Korean J. Physiol. Pharmacol. Off. J. Korean Physiol. Soc. Korean Soc. 2017, 21, 169. [Google Scholar] [CrossRef]
- Zhou, D.; Wang, L.; Cui, Q.; Iftikhar, R.; Xia, Y.; Xu, P. Repositioning lidocaine as an anticancer drug: The role beyond anesthesia. Cell Dev. Biol. 2020, 8, 565. [Google Scholar] [CrossRef]
- Wu, K.-C.; Liao, K.-S.; Yeh, L.-R.; Wang, Y.-K. Drug repurposing: The mechanisms and signaling pathways of anticancer effects of anesthetics. Biomedicines 2022, 10, 1589. [Google Scholar] [CrossRef] [PubMed]
- Lourenço, T.; Vale, N. Pharmacological efficacy of repurposing drugs in the treatment of prostate cancer. J. Mol. Sci. 2023, 24, 4154. [Google Scholar] [CrossRef] [PubMed]
- Alfaqih, M.A.; Nelson, E.R.; Liu, W.; Safi, R.; Jasper, J.S.; Macias, E.; Geradts, J.; Thompson, J.W.; Dubois, L.G.; Freeman, M.R.; et al. CYP27A1 loss dysregulates cholesterol homeostasis in prostate cancer. Cancer Res. 2017, 77, 1662–1673. [Google Scholar] [CrossRef] [PubMed]
- Geng, X.; Wang, F.; Tian, D.; Huang, L.; Streator, E.; Zhu, J.; Kurihara, H.; He, R.; Yao, X.; Zhang, Y.; et al. Cardiac glycosides inhibit cancer through Na/K-ATPase-dependent cell death induction. Pharmacol. 2020, 182, 114226. [Google Scholar] [CrossRef]
- Arend, R.C.; Londoño-Joshi, A.I.; Gangrade, A.; Katre, A.A.; Kurpad, C.; Li, Y.; Samant, R.S.; Li, P.-K.; Landen, C.N.; Yang, E.S.; et al. Niclosamide and its analogs are potent inhibitors of Wnt/β-catenin, mTOR and STAT3 signaling in ovarian cancer. Oncotarget 2016, 7, 86803. [Google Scholar] [CrossRef]
- Wang, J.; Ren, X.-R.; Piao, H.; Zhao, S.; Osada, T.; Premont, R.T.; Mook, R.A.; Morse, M.A.; Lyerly, H.K.; Chen, W. Niclosamide-induced Wnt signaling inhibition in colorectal cancer is mediated by autophagy. J. 2019, 476, 535–546. [Google Scholar] [CrossRef]
- Hamilton, G.; Rath, B. Repurposing of anthelminthics as anticancer drugs. Oncomedicine 2018, 3, 1–8. [Google Scholar] [CrossRef]
- Mussin, N.; Oh, S.C.; Lee, K.-W.; Park, M.Y.; Seo, S.; Yi, N.-J.; Kim, H.; Yoon, K.C.; Ahn, S.-W.; Kim, H.-S.; et al. Sirolimus and metformin synergistically inhibits colon cancer in vitro and in vivo. Korean Med. Sci. 2017, 32, 1385–1395. [Google Scholar] [CrossRef]
- Sanchez-Plumed, J.A.; Molina, M.G.; Alonso, A.; Arias, M. Sirolimus, the first mTOR inhibitor. Nefrología 2006, 26, 21–32. [Google Scholar]
- Granata, S.; Mercuri, S.; Troise, D.; Gesualdo, L.; Stallone, G.; Zaza, G. mTOR-inhibitors and post-transplant diabetes mellitus: A link still debated in kidney transplantation. Med. 2023, 10, 1168967. [Google Scholar] [CrossRef]
- Kalyanaraman, B.; Cheng, G.; Hardy, M.; Ouari, O.; Sikora, A.; Zielonka, J.; Dwinell, M.B. Modified metformin as a more potent anticancer drug: Mitochondrial inhibition, redox signaling, antiproliferative effects and future EPR studies. Cell Biochem. Biophys. 2017, 75, 311–317. [Google Scholar] [CrossRef] [PubMed]
- Cheng, G.; Zielonka, J.; Ouari, O.; Lopez, M.; McAllister, D.; Boyle, K.; Barrios, C.S.; Weber, J.J.; Johnson, B.D.; Hardy, M.; et al. Mitochondria-targeted analogues of metformin exhibit enhanced antiproliferative and radiosensitizing effects in pancreatic cancer cells. Cancer Res. 2016, 76, 3904–3915. [Google Scholar] [CrossRef]
- Amengual-Cladera, E.; Morla-Barcelo, P.M.; Morán-Costoya, A.; Sastre-Serra, J.; Pons, D.G.; Valle, A.; Roca, P.; Nadal-Serrano, M. Metformin: From Diabetes to Cancer—Unveiling Molecular Mechanisms and Therapeutic Strategies. Biology 2024, 13, 302. [Google Scholar] [CrossRef] [PubMed]
- Raafat, S.N.; El Wahed, S.A.; Badawi, N.M.; Saber, M.M.; Abdollah, M.R. Enhancing the anticancer potential of metformin: Fabrication of efficient nanospanlastics, in vitro cytotoxic studies on HEP-2 cells and reactome enhanced pathway analysis. Int. J. Pharm. X 2023, 6, 100215. [Google Scholar] [CrossRef]
- Pinto, L.C.; Mesquita, F.P.; Soares, B.M.; da Silva, E.L.; Puty, B.; de Oliveira, E.H.C.; Burbano, R.R.; Montenegro, R.C. Mebendazole induces apoptosis via C-MYC inactivation in malignant ascites cell line (AGP01). Toxicol. Vitr. 2019, 60, 305–312. [Google Scholar] [CrossRef] [PubMed]
- Chai, J.-Y.; Jung, B.-K.; Hong, S.-J. Albendazole and mebendazole as anti-parasitic and anticancer agents: An update. Korean J. Parasitol. 2021, 59, 189. [Google Scholar] [CrossRef] [PubMed] [PubMed Central]
- Aminzadeh-Gohari, S.; Weber, D.D.; Vidali, S.; Catalano, L.; Kofler, B.; Feichtinger, R.G. From old to new—Repurposing drugs to target mitochondrial energy metabolism in cancer. Semin. Cell Dev. Biol. 2020, 98, 211–223. [Google Scholar] [CrossRef] [PubMed]
- Wang, S.-F.; Tseng, L.-M.; Lee, H.-C. Role of mitochondrial alterations in human cancer progression and cancer immunity. J. Biomed. Sci. 2023, 30, 61. [Google Scholar] [CrossRef]
- Yang, Y.; An, Y.; Ren, M.; Wang, H.; Bai, J.; Du, W.; Kong, D. The mechanisms of action of mitochondrial targeting agents in cancer: Inhibiting oxidative phosphorylation and inducing apoptosis. Pharmacol. 2023, 14, 1243613. [Google Scholar] [CrossRef]
- Wang, J.; Sun, D.; Huang, L.; Wang, S.; Jin, Y. Targeting reactive oxygen species capacity of tumor cells with repurposed drug as an anticancer therapy. Oxidative Med. Cell. Longev. 2021, 2021, 8532940. [Google Scholar] [CrossRef]
- Yadav, V.; Talwar, P. Repositioning of fluoroquinolones from antibiotic to anticancer agents: An underestimated truth. Pharmacother. 2019, 111, 934–946. [Google Scholar] [CrossRef] [PubMed]
- Thiruchenthooran, V.; Sánchez-López, E.; Gliszczyńska, A. Perspectives of the application of non-steroidal anti-inflammatory drugs in cancer therapy: Attempts to overcome their unfavorable side effects. Cancers 2023, 15, 475. [Google Scholar] [CrossRef] [PubMed]
- Duarte, D.; Vale, N. Antidepressant drug sertraline against human cancer cells. Biomolecules 2022, 12, 1513. [Google Scholar] [CrossRef]
- Peixoto, R.; Pereira, M.d.L.; Oliveira, M. Beta-blockers and cancer: Where are we? Pharmaceuticals 2020, 13, 105. [Google Scholar] [CrossRef]
- Ma, S.-N.; Mao, Z.-X.; Wu, Y.; Liang, M.-X.; Wang, D.-D.; Chen, X.; Chang, P.-A.; Zhang, W.; Tang, J.-H. The anticancer properties of heparin and its derivatives: A review and prospect. Cell Adhes. Migr. 2020, 14, 118–128. [Google Scholar] [CrossRef]
- Rawla, P. Epidemiology of prostate cancer. World J. Oncol. 2019, 10, 63. [Google Scholar] [CrossRef] [PubMed]
- Bahmad, H.F.; Demus, T.; Moubarak, M.M.; Daher, D.; Moreno, J.C.A.; Polit, F.; Lopez, O.; Merhe, A.; Abou-Kheir, W.; Nieder, A.M.; et al. Overcoming drug resistance in advanced prostate cancer by drug repurposing. Sci. 2022, 10, 15. [Google Scholar] [CrossRef] [PubMed]
- Araújo, D.; Ribeiro, E.; Amorim, I.; Vale, N. Repurposed drugs in gastric cancer. Molecules 2022, 28, 319. [Google Scholar] [CrossRef]
- Fatemi, N.; Karimpour, M.; Bahrami, H.; Zali, M.R.; Chaleshi, V.; Riccio, A.; Nazemalhosseini-Mojarad, E.; Totonchi, M. Current trends and future prospects of drug repositioning in gastrointestinal oncology. Pharmacol. 2024, 14, 1329244. [Google Scholar] [CrossRef]
- Mu, J.; Xu, H.; Yang, Y.; Huang, W.; Xiao, J.; Li, M.; Tan, Z.; Ding, Q.; Zhang, L.; Lu, J.; et al. Thioridazine, an antipsychotic drug, elicits potent antitumor effects in gastric cancer. Rep. 2014, 31, 2107–2114. [Google Scholar] [CrossRef]
- Yang, Z.-Y.; Zhao, Y.-W.; Xue, J.-R.; Guo, R.; Zhao, Z.; Liu, H.-D.; Ren, Z.-G.; Shi, M. Thioridazine reverses trastuzumab resistance in gastric cancer by inhibiting S-phase kinase associated protein 2-mediated aerobic glycolysis. World J. Gastroenterol. 2023, 29, 5974. [Google Scholar] [CrossRef] [PubMed]
- Bedford, M.R.; Ford, S.J.; Horniblow, R.D.; Iqbal, T.H.; Tselepis, C. Iron chelation in the treatment of cancer: A new role for deferasirox? Clin. Pharmacol. 2013, 53, 885–891. [Google Scholar] [CrossRef]
- Stewart, A.K. How Thalidomide Works Against Cancer. Science 2014, 343, 256–257. [Google Scholar] [CrossRef] [PubMed]
- Kale, V.P.; Habib, H.; Chitren, R.; Patel, M.; Pramanik, K.C.; Jonnalagadda, S.C.; Challagundla, K.; Pandey, M.K. Old drugs, new uses: Drug repurposing in hematological malignancies. Cancer Biol. 2020, 68, 242–248. [Google Scholar] [CrossRef] [PubMed]
- Licht, J.D.; Shortt, J.; Johnstone, R. From anecdote to targeted therapy: The curious case of thalidomide in multiple myeloma. Cancer Cell 2014, 25, 9–11. [Google Scholar] [CrossRef]
- Al Khzem, A.H.; Gomaa, M.S.; Alturki, M.; Tawfeeq, N.; Sarafroz, M.; Alonaizi, S.; Al Faran, A.; Alrumaihi, L.; Alansari, F.; Alghamdi, A. Rebirth of thalidomide. World J. Pharm. Res. 2022, 11, 842–854. [Google Scholar]
- Iqbal, N.; Iqbal, N. Imatinib: A breakthrough of targeted therapy in cancer. Res. Pract. 2014, 2014, 357027. [Google Scholar] [CrossRef]
- Phuar, H.L.; Begley, C.E.; Chan, W.; Krause, T.M. Tyrosine kinase inhibitors initiation, cost sharing, and health care utilization in patients with newly diagnosed chronic myeloid leukemia: A retrospective claims-based study. Manag. Care Spec. Pharm. 2019, 25, 1140–1150. [Google Scholar] [CrossRef]
- Jabbour, E.; Kantarjian, H. Chronic myeloid leukemia: 2018 update on diagnosis, therapy and monitoring. J. Hematol. 2018, 93, 442–459. [Google Scholar] [CrossRef]
- Senapati, J.; Jabbour, E.; Kantarjian, H.; Short, N.J. Pathogenesis and management of accelerated and blast phases of chronic myeloid leukemia. Leukemia 2023, 37, 5–17. [Google Scholar] [CrossRef]
- Anjum, S.; Naseer, F.; Ahmad, T.; Jahan, F.; Qadir, H.; Gul, R.; Kousar, K.; Sarwar, A.; Shabbir, A. Enhancing therapeutic efficacy: Sustained delivery of 5-fluorouracil (5-FU) via thiolated chitosan nanoparticles targeting CD44 in triple-negative breast cancer. Rep. 2024, 14, 11431. [Google Scholar] [CrossRef]
- Shivani, D.; Misari, P.; Anand, N.; Nandita, C.; Jignesh, S. Drug repurposing: A retrospective revolution in breast cancer medicine. Med. 2024, 1, 11. [Google Scholar] [CrossRef]
- Zhang, Q.; Wang, S.; Yang, D.; Pan, K.; Li, L.; Yuan, S. Preclinical pharmacodynamic evaluation of antibiotic nitroxoline for anticancer drug repurposing. Lett. 2016, 11, 3265–3272. [Google Scholar] [CrossRef] [PubMed]
- El Zarif, T.; Yibirin, M.; De Oliveira-Gomes, D.; Machaalani, M.; Nawfal, R.; Bittar, G.; Bahmad, H.F.; Bitar, N. Overcoming therapy resistance in colon cancer by drug repurposing. Cancers 2022, 14, 2105. [Google Scholar] [CrossRef]
- Qi, J.; Bhatti, P.; Spinelli, J.J.; Murphy, R.A. Antihypertensive medications and risk of colorectal cancer in British Columbia. Pharmacol. 2023, 14, 1301423. [Google Scholar] [CrossRef]
- Kedika, R.; Patel, M.; Sahdala, H.N.P.; Mahgoub, A.; Cipher, D.; Siddiqui, A.A. Long-term use of angiotensin converting enzyme inhibitors is associated with decreased incidence of advanced adenomatous colon polyps. Clin. Gastroenterol. 2011, 45, e12–e16. [Google Scholar] [CrossRef]
- Massalee, R.; Cao, X. Repurposing beta-blockers for combinatory cancer treatment: Effects on conventional and immune therapies. Pharmacol. 2024, 14, 1325050. [Google Scholar] [CrossRef] [PubMed]
- Jiang, G.; Zhou, X.; Hu, Y.; Tan, X.; Wang, D.; Yang, L.; Zhang, Q.; Liu, S. The antipsychotic drug pimozide promotes apoptosis through the RAF/ERK pathway and enhances autophagy in breast cancer cells. Cancer Biol. Ther. 2024, 25, 2302413. [Google Scholar] [CrossRef] [PubMed]
- Chen, J.; Zhang, L.; Cai, N.; Zhang, Z.; Ji, K. Antipsychotic agent pimozide promotes reversible proliferative suppression by inducing cellular quiescence in liver cancer. Oncol. Rep. 2019, 42, 1101–1109. [Google Scholar] [CrossRef]
- Attia, Y.M.; Ewida, H.; Ahmed, M.S. Successful Stories of Drug Repurposing for Cancer Therapy in Hepatocellular Carcinoma. Drug Repurposing in Cancer Therapy; Academic Press: Cambridge, MA, USA, 2020; pp. 213–229. [Google Scholar] [CrossRef]
- Huang, S.-T.; Hsu, W.-F.; Huang, H.-S.; Yen, J.-H.; Lin, M.-C.; Peng, C.-Y.; Yen, H.-R. Improved survival in hepatocellular carcinoma patients with cardiac arrhythmia by amiodarone treatment through autophagy. J. Mol. Sci. 2019, 20, 3978. [Google Scholar] [CrossRef]
- Chao, M.-W.; Chen, T.-H.; Huang, H.-L.; Chang, Y.-W.; HuangFu, W.-C.; Lee, Y.-C.; Teng, C.-M.; Pan, S.-L. Lanatoside C, a cardiac glycoside, acts through protein kinase Cδ to cause apoptosis of human hepatocellular carcinoma cells. Rep. 2017, 7, 46134. [Google Scholar] [CrossRef] [PubMed]
- Gao, X.; Liu, X.; Shan, W.; Liu, Q.; Wang, C.; Zheng, J.; Yao, H.; Tang, R.; Zheng, J. Anti-malarial atovaquone exhibits anti-tumor effects by inducing DNA damage in hepatocellular carcinoma. J. Cancer Res. 2018, 8, 1697. [Google Scholar] [PubMed] [PubMed Central]
- Stevens, A.M.; Schafer, E.S.; Li, M.; Terrell, M.; Rashid, R.; Paek, H.; Bernhardt, M.B.; Weisnicht, A.; Smith, W.T.; Keogh, N.J.; et al. Repurposing atovaquone as a therapeutic against acute myeloid leukemia (AML): Combination with conventional chemotherapy is feasible and well tolerated. Cancers 2023, 15, 1344. [Google Scholar] [CrossRef] [PubMed]
- Kumavath, R.; Paul, S.; Pavithran, H.; Paul, M.K.; Ghosh, P.; Barh, D.; Azevedo, V. Emergence of cardiac glycosides as potential drugs: Current and future scope for cancer therapeutics. Biomolecules 2021, 11, 1275. [Google Scholar] [CrossRef]
- Kim, U.; Kim, C.-Y.; Lee, J.M.; Ryu, B.; Kim, J.; Shin, C.; Park, J.-H. Pimozide inhibits the human prostate cancer cells through the generation of reactive oxygen species. Front. Pharmacol. 2020, 10, 1517. [Google Scholar] [CrossRef]
- Dakir, E.-H.; Pickard, A.; Srivastava, K.; McCrudden, C.M.; Gross, S.R.; Lloyd, S.; Zhang, S.-D.; Margariti, A.; Morgan, R.; Rudland, P.S.; et al. The anti-psychotic drug pimozide is a novel chemotherapeutic for breast cancer. Oncotarget 2018, 9, 34889–34910. [Google Scholar] [CrossRef]
- Greene, J.; Segaran, A.; Lord, S. Targeting OXPHOS and the electron transport chain in cancer; Molecular and therapeutic implications. Semin. Cancer Biol. 2022, 86, 851–859. [Google Scholar] [CrossRef]
- Fiorillo, M.; Lamb, R.; Tanowitz, H.B.; Mutti, L.; Krstic-Demonacos, M.; Cappello, A.R.; Martinez-Outschoorn, U.E.; Sotgia, F.; Lisanti, M.P. Repurposing atovaquone: Targeting mitochondrial complex III and OXPHOS to eradicate cancer stem cells. Oncotarget 2016, 7, 34084. [Google Scholar] [CrossRef]
- Basak, D.; Gamez, D.; Deb, S. SGLT2 inhibitors as potential anticancer agents. Biomedicines 2023, 11, 1867. [Google Scholar] [CrossRef]
- Papadopoli, D.; Uchenunu, O.; Palia, R.; Chekkal, N.; Hulea, L.; Topisirovic, I.; Pollak, M.; St-Pierre, J. Perturbations of cancer cell metabolism by the antidiabetic drug canagliflozin. Neoplasia 2021, 23, 391–399. [Google Scholar] [CrossRef]
- Jin, P.; Jiang, J.; Zhou, L.; Huang, Z.; Nice, E.C.; Huang, C.; Fu, L. Mitochondrial adaptation in cancer drug resistance: Prevalence, mechanisms, and management. J. Hematol. Oncol. 2022, 15, 97. [Google Scholar] [CrossRef] [PubMed]
- Schultz, C.W.; Nevler, A. Pyrvinium pamoate: Past, present, and future as an anticancer drug. Biomedicines 2022, 10, 3249. [Google Scholar] [CrossRef] [PubMed]
- Tomitsuka, E.; Kita, K.; Esumi, H. An anticancer agent, pyrvinium pamoate inhibits the NADH–fumarate reductase system—A unique mitochondrial energy metabolism in tumour microenvironments. J. Biochem. 2012, 152, 171–183. [Google Scholar] [CrossRef] [PubMed]
- Weng, N.; Zhang, Z.; Tan, Y.; Zhang, X.; Wei, X.; Zhu, Q. Repurposing antifungal drugs for cancer therapy. J. Adv. Res. 2023, 48, 259–273. [Google Scholar] [CrossRef]
- Tsubamoto, H.; Ueda, T.; Inoue, K.; Sakata, K.; Shibahara, H.; Sonoda, T. Repurposing itraconazole as an anticancer agent. Oncol. Lett. 2017, 14, 1240–1246. [Google Scholar] [CrossRef]
- Head, S.A.; Shi, W.; Zhao, L.; Gorshkov, K.; Pasunooti, K.; Chen, Y.; Deng, Z.; Li, R.-J.; Shim, J.S.; Tan, W.; et al. Antifungal drug itraconazole targets VDAC1 to modulate the AMPK/mTOR signaling axis in endothelial cells. Proc. Natl. Acad. Sci. USA 2015, 112, E7276–E7285. [Google Scholar] [CrossRef]
- Pancu, D.F.; Scurtu, A.; Macasoi, I.G.; Marti, D.; Mioc, M.; Soica, C.; Coricovac, D.; Horhat, D.; Poenaru, M.; Dehelean, C. Antibiotics: Conventional therapy and natural compounds with antibacterial activity—A pharmaco-toxicological screening. Antibiotics 2021, 10, 401. [Google Scholar] [CrossRef]
- Stokes, J.M.; Yang, K.; Swanson, K.; Jin, W.; Cubillos-Ruiz, A.; Donghia, N.M.; Macnair, C.R.; French, S.; Carfrae, L.A.; Bloom-Ackermann, Z.; et al. A deep learning approach to antibiotic discovery. Cell 2020, 180, 688–702. [Google Scholar] [CrossRef]
- Bano, N.; Parveen, S.; Saeed, M.; Siddiqui, S.; Abohassan, M.; Mir, S.S. Drug Repurposing of Selected Antibiotics: An Emerging Approach in Cancer Drug Discovery. ACS Omega 2024, 9, 26762–26779. [Google Scholar] [CrossRef]
- Castro, L.; Kviecinski, M.; Ourique, F.; Parisotto, E.; Grinevicius, V.; Correia, J.; Filho, D.W.; Pedrosa, R. Albendazole as a promising molecule for tumor control. Redox Biol. 2016, 10, 90–99. [Google Scholar] [CrossRef]
Файлы
Какова ваша реакция?